不太可能遗传嫌疑嫌疑人涉及共同的大脑缺陷
遗传搜索从患者到小鼠模型缠绕的遗传搜索并返回患者已经发现了一个不太可能的基因,统治性涉及常见的出生缺陷,导致精神发育迟滞,运动延迟和有时自闭症,为这种疾病提供了新的机制和可能改善治疗。
芝加哥大学,艾伯塔大学和其他机构的研究人员在9月份宣布自然遗传学FOXC1基因导致Dandy-Walker畸形(DWM), a脑缺陷每5000个新生儿中就有一个会出现这种情况。
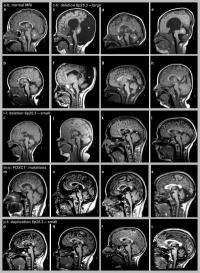
丹迪-沃克畸形基因的作用消除了关于先天患有该疾病的儿童大脑中什么地方出错的迷雾。DWM的特点是小脑形成不正常,小脑位于大脑后部,参与运动和协调。因此,患有这种疾病的儿童需要大量的医疗护理,在某些情况下需要手术来治疗大脑周围的积液,这种情况被称为脑积水。
研究人员惊讶地发现FoxC1基因介导小脑的发育并导致DWM,因为基因永远不会在大脑本身中表达。相反,FoxC1基因在胎儿组织中表达,称为间充质,形成围绕和保护脑的颅骨和其他层。这种机制表明胚胎的令人兴奋的新元素大脑发育凯瑟琳·米伦博士是该研究的合著者,也是马里兰大学的助理教授人类遗传学在芝加哥大学。
“大脑周围的所有东西都对大脑本身的大脑发展具有重要的是重要的,”Millen说。
在显影胎儿中,FOXC1充当“母部调节因子”,指导其他基因的表达,反过来给出相邻胚胎大脑所必需的指令。
“它是控制下游基因,我们所知的一些下游基因是信号分子和生长因子,显然是脑发展所必需的,”Millen说。“当你没有他们时,大脑被搞砸了;不是因为致病基因在大脑中表达但是因为它在周围组织中。”
这个新的发现是在2004年发表的同一组研究中发现的第一个与DWM相关的基因之后。
"The first gene didn't give us a huge clue, but this one gives us a major clue to the underlying cause," said study co-author William Dobyns, M.D., professor of Human Genetics, Neurology and Pediatrics at the University of Chicago.
在研究人员发表于与该疾病相关的前两种基因上,2004年,不太可能的FoxC1基因的路径开始于2004年提到Dobyns的Dandy-Walker患者。虽然这些基因位于3染色体上,但该患者表现出异常的染色体6,暗示DWM的第二热点。
研究人员将搜索结果缩小到染色体八个基因的区域6.患有严重DWM的患者在目标区域中缺少多达七种基因,而缺少一个基因的患者只有MRI脑扫描才能检测到轻度异常。
为了确定八个基因在疾病的发展中最关键,研究人员转向小鼠模型。一只小鼠选择性地缺乏FoxC1基因,以研究眼睛,心脏和肌肉缺陷,但没有人研究过大脑。
•米伦说,她怀疑自己鼠标缺乏FOXC1基因会与他们的研究,和她打赌金伯利Aldinger说,芝加哥大学的神经生物学研究生是这项研究的第一作者,免费的午餐,他们寻求的基因并不是一个。她很高兴地输掉了这个赌注。
“当我们看着第一个大脑的那一刻,它是如此明显,他们有一个非常搞砸的小脑,它已经完全被忽视了,”米兰说。
现在相信Foxc1对小鼠的小脑发育很重要,研究人员然后搜索缺乏全部或部分基因的人类。幸运的是,他们在艾伯塔大学的眼科和医学遗传学副教授曾经发现了11名来自Ordan Lehmann的科目,他正在研究由Foxc1引起的儿科发病青光眼患者。
当青光眼患者获得MRI扫描时,研究人员观察了大脑异常,证明了FOXC1参与了令人愉快的助行者畸形。
米伦说:“这些患者是将大脑畸形归咎于FOXC1基因的关键。”“基于小鼠突变体,我们非常怀疑这一定是FOXC1,患者也证实了这一点。”
青光眼是一种常见的疾病,以前被认为仅仅是一种视神经疾病——连接眼睛和大脑的神经。对FOXC1基因如何指导小脑和其他大脑结构发展的进一步研究,也可能为脑积水、自闭症和其他疾病带来新的研究途径和治疗方法。
“现在我们了解了发生了什么,我们可以看看所有其他位点,看看是否有其他基因符合这个框架,”米伦说。“从现在开始,基因发现应该会快得多,因为我们了解了基本的生物学原理。”
“这一发现让我们重新思考这种疾病的基础,”约瑟夫·格里森医学博士说,他是加州大学圣地亚哥分校霍华德·休斯医学研究所的一名研究员,他没有参与这项研究。“这将是一个转变,从我们思考它的方式,到一个新的范式,有一大堆新的想法,我们如何理解丹迪-沃克畸形。”
资料来源:芝加哥大学医学中心
进一步探索











用户评论