科学家揭示了普通艾滋病毒子组中关键蛋白质的结构
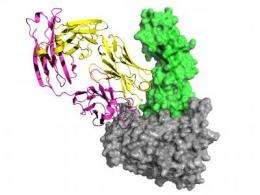
来自加州理工学院的科学家们已经提供了首次瞥见了一个关键蛋白质 - GP120的结构 - 在人类免疫缺陷病毒的特定亚组表面,HIV-1中发现。此外,它们证明了GP120的特定抗体不仅与蛋白质接触,而且与CD4受体一起接触GP120用于增加体内T细胞的入口。
这三维了解GP120如何构建的不仅仅是基本的科学进步。“开发疫苗有巨大的持续努力艾滋病病毒,“Caltech Proddoctoral Scholar Ron Diskin说,”大多数努力都使用GP120。拥有更多结构信息将有助于更好的疫苗设计。“
该调查结果详述了在期刊上发表的论文中自然结构和分子生物学。
研究小组特别研究了来自C型HIV-1的gp120。为了解释这是什么意思,这里有一个简短的艾滋病毒家族历史:大多数人感染了艾滋病毒并继续艾滋病是感染了艾滋病毒1家族的成员。HIV-1被分为若干组;大多数与艾滋病相关的病毒株来自m组,这些组又进一步细分为我们所知的支系。
CLADE B是美国和西欧最常发现的M艾滋病毒1组的形式,以及可能最适合迄今为止的人。Clade C,Caltech团队研究的Clade是“一个毁灭性的非洲和亚洲的人,”Diskin说。“这是一个可能导致全世界最多感染的人。”
以前的研究看过Clade B GP120的结构,并且已经假设 - 但不是证明 - Clade C的版本看起来很差。
为了揭示Clade C GP120的结构 - 并确定关于其相似性的假设是否确实是真实的,所以CALTECH团队需要结晶蛋白质。这不是一件容易的任务。结果表明,Diskin,蛋白质本身并不足够坚硬以结晶。因此,研究人员创造了由称为21℃的GP120单体,CD4受体和抗HIV抗体组成的分子复合物。
这种配置促进了结晶,并允许科学家不仅看着GP120 - 这实际上,“在CLADE B中的Clade C看起来与Clade B中的看起来相同,”Diskin-ant,但要想象整个装订网站,看看如何复杂的各种组件彼此相互作用。
就在那时,他们发现了一些不寻常的现象:抗体21c不仅对从HIV包膜上伸出的gp120蛋白产生反应(从而与之接触),而且还对人体自身的CD4受体产生反应T细胞。这种多反应性——对一种以上抗原的反应——首次在hiv抗体的3-D结构中显现出来。
“我们结构中最有趣的方面是抗体和CD4之间的意外接触,”Caltech Max Delbruck Biology教授Pamela Bjorkman说,霍华德休斯医学院调查员和Caltech团队的领导者。“与CD4的结合表明这类抗HIV抗体具有自身反应性,这提出了许多有趣的问题,即抗艾滋病毒免疫反应如何影响hiv感染者。”
这种自动反应性是否意味着21C无法与之合作,因为临床医生可能会掌握潜在的自身免疫反应,其疫苗引起21c样抗体?
不一定是,Diskin说。
“其他数据显示,一些最好的中和抗体也是自身反应性的,”他解释说。
然而,它的意思是克服这种抗体反应克服的额外障碍是额外的障碍。该体倾向于消除自动反应性抗体,以试图在海湾保持自身免疫性疾病。“为了创造一个良好的疫苗来生产21℃的抗体,研究人员将不得不克服这种消除机制。”
加州理工学院团队的下一步是尝试改进本文中提出的相对低分辨率的结构。此外,Diskin说,该团队还想尝试解决gp120三聚体的结构,这是一种更复杂的三叉蛋白。
进一步探索






用户评论