研究表明胎儿心脏发育的关键酶也与成人心脏病有关
斯坦福大学医学院的科学家们首次发现了一种酶,这种酶在胎儿心脏发育和导致成人心脏肥大(心脏增大)方面都起着至关重要的作用。这一发现可以在未来用于开发治疗心脏病的新疗法。
这项研究将于7月1日发表在自然,由心血管医学助理教授、医学博士张庆平(Ching-Pin Chang)和他的实验室进行,该实验室研究心脏发育机制,并花了数年时间研究胚胎心脏发育和成人心脏病的表观遗传学基础。(在生物学中,特别是在遗传学中,表观遗传学是对遗传变化的研究基因表达而不是由底层DNA序列的变化引起的。)
伴随着细胞的增生性生长心肌当成人心脏受到高血压等各种伤害时,就会出现纤维化或瘢痕。这最终会导致心脏衰竭。Chang和他的同事们发现,一种叫做BAF的蛋白质复合物中的Brg1酶在触发这一过程中起着关键的表观遗传作用。Brg1/BAF蛋白复合物改变了DNA包裹组蛋白的方式,从而影响了细胞的发育。
在对小鼠胎心的研究中,Chang实验室发现Brg1调节胎儿心肌细胞增殖而分化和维持胎儿心肌处于“胚胎”状态。在缺少Brg1的情况下,胎儿心肌细胞失去了胚胎的特征,呈现出“成人”细胞的特征。
“我们发现Brg1通过打开/关闭特定的肌肉基因,在小鼠胚胎心脏发育中发挥着重要作用,”Chang实验室的研究生、该研究的第一作者Calvin Hang说。“因为患病的成人心脏经常会打开本应关闭的胎儿基因,我们想知道Brg1是否也在成人心脏病中发挥作用。”
“与胚胎不同,Brg1基因在正常成人心肌(心肌)中是关闭的,”该研究的资深作者Chang说。这种酶在心脏成熟时自然消失。“但它会在心脏压力下重新激活。”
科学家们发现,在压力较大的成人心脏中,Brg1的重新激活会触发一个细胞过程,从而激活那些在成人心脏中通常是沉默的胎儿基因。这就导致了疾病。
因此,研究人员检查了如果Brg1酶被敲除,这种疾病过程——成人心脏肥大——是否会发生。
就像对小鼠胎儿心脏的实验一样,科学家们使用组织特异性和时间控制的基因敲除技术来消除成年小鼠心脏中的Brg1基因,然后对这些心脏施加物理压力,以观察是否发生疾病。他们发现心脏肥厚的数量显著减少。
Chang说:“当Brg1基因被删除时,应激成年小鼠心脏只有极小的病理变化。”“它没有明显的肥大。没有纤维化或疤痕。”
当Brg1/BAF在小鼠的成年心脏中被心脏应激激活时,它与另外两个表观遗传因子HDAC和PARP组装了一个大的蛋白质复合物,以控制心肌的生长和分化,就像它们通常在胎儿心脏中所做的那样,只是这个胎儿复合物现在在成年细胞中起作用。这导致小鼠心脏肥大和纤维化。
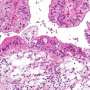
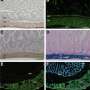
Chang和他的同事们更进一步,在斯坦福心血管基因组学和蛋白质组学组织库冷藏的人类心脏组织中,小规模地检查了Brg1基因的激活。实验中使用了4名原因不明的肥厚性心肌病患者的心脏组织,以及6个来自移植供体心脏的健康心脏样本。他们发现,在应激的成年小鼠心脏中观察到的Brg1,在肥厚性心肌病患者的心脏中被激活。这些患者的Brg1激活水平与疾病的严重程度密切相关。
Chang说:“这是一项开创性的研究,但结果令人鼓舞。”
这些观察结果表明,Brg1激活可能有助于某些人类肥厚的发展心疾病。Chang说:“我们希望开发一种化学抑制剂,可以针对肥厚性心脏中的Brg1活性,并治疗这种疾病。”