FDA可能会限制贫血药物用于肾脏疾病
(AP) - 食品药品监督管理局正在考虑对广泛使用的贫血药物的新限制,这些药物似乎是肾脏疾病患者中风的风险的两倍。
FDA周四发布了对Amgen Inc.的三种促进血液促进药物的安全审查,重点是他们在慢性患者中的使用肾脏疾病他们病还不够生病,无法接受透析。
药品 - 宠儿,Aranesp和Epogen-是数十亿美元的销售商,因为它们能够增强氧气携带红细胞,减少对输血的需求。但是自2007年以来,销售额就急剧下降,当时FDA在药物中添加了几个安全警告中的第一个,基于证据,它们可能导致肿瘤生长并加速癌症患者死亡。这些药物不再用于患有几种类型的癌症的患者。
贫血会导致无力和呼吸急促,是化学疗法和肾功能衰竭。
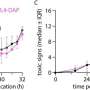
现在,FDA正在审查去年发表的一项研究,该研究表明,服用ARANESP的肾脏疾病患者与服用虚拟治疗的肾脏疾病患者的中风可能是两倍。该研究的目的是表明该药物可以防止心脏病发作,中风和其他与心脏有关的问题,如多年来所假定。
但是FDA审稿人使用Aranesp的化学名称在其文章中说:“证据对以这种方式使用darbepoetin的安全性和建议性产生了极大的怀疑。”
安进认为应该继续使用其药物,因为它们有助于避免输血,而输血会带来自身的风险。但是FDA的科学家指出,服用该公司药物的患者中有15%仍需要输血,而服用的患者中有25%安慰剂治疗。
FDA综述说:“治疗并没有消除需要(红细胞)输血的风险。”
周一,该机构将要求由外部专家组成的小组审查数据,并就如何安全使用这些药物提出建议。小组成员可以推荐加固的警告标签,其他研究或较低剂量的药物。尽管经常这样做,但不需要FDA遵循该小组的建议。
总部位于加利福尼亚州千橡市的Amgen生产所有三种药物。Procrit由Johnson&Johnson的Centocor Ortho Biotech部门出售,根据两家公司之间的长期协议。
根据健康数据公司IMS Health的数据,去年,这些药物(称为促红细胞生成的药物刺激药物)的销售额为63亿美元。
德意志银行的分析师Robyn Karneuskas估计,去年透析前肾脏患者占ARANESP收入的30%。他估计,新的FDA限制将使该药物的销售额减少8600万美元,这对Amgen的收入产生的影响最小。Amgen是生物技术制药行业的巨头之一,去年的总收入超过146亿美元。
进一步探索
©2010美联社。版权所有。该材料可能不会出版,广播,重写或重新分布。