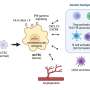
用于骨骼扫描的新药获批
FDA已经批准了美国国立卫生研究院下属的国家癌症研究所(NCI)的一项新药申请(NDA),用于先前批准的一种药物氟化钠F18的新强度,用于骨骼扫描。与锝-99m (Tc-99m)相比,氟化钠F18不受导致最近全国Tc-99m短缺的供应问题的影响。Tc-99m是唯一被批准用于骨骼扫描的放射性示踪剂。
许多诊断成像测试,包括使用单光子发射计算机断层扫描(SPECT)的骨骼扫描,需要使用Tc-99m。骨骼扫描是诊断前列腺癌的重要工具骨转移癌症患者,特别是那些癌症(如乳腺癌和前列腺癌)倾向于转移到骨骼的患者。氟化钠F18于1972年获得批准,但在1975年被撤销,当时更便宜的示踪剂Tc-99m问世。Tc-99m来源于钼-99 (Mo-99)的同位素,这种同位素主要在高浓缩铀核反应堆中制造。由于Mo-99和Tc-99m的半衰期都相当短(分别为66小时和6小时),这些药物不能储存。
目前全球有7个核反应堆生产Mo-99用于医疗用途,其中美国的大部分供应来自中国核反应堆在加拿大,该公司经常停电,最近一次停电持续了一年多。尽管氟化钠F18比Tc-99更贵,但它可以在美国许多学术大学和商业供应商提供的医用回旋加速器中生产。这种药物还可以提供更好的图像,因为它使用位置发射断层扫描(PET)而不是SPECT成像,可以改进,更早地检测。
之前氟化钠F18的剂量停产是出于市场原因,而不是出于安全性或有效性的原因。NCI希望多家公司和机构提交缩写新药申请(anda),这样就可以生产这种药物的仿制药,从而降低成本。2010年2月26日,医疗保险和医疗补助服务中心发布了一项关于氟化钠PET扫描覆盖范围的决定。它允许证据开发覆盖(CED),国家肿瘤PET登记处(NOPR)正在建立一个正式的登记处,这应该有助于促进这一覆盖。
进一步探索