在肥胖的人肠道微生物网络不同于规范,揭示了系统生物学方法
第一次,研究人员分析了许多居住在人类肠道微生物复杂,综合生物系统,而不是一组单独的物种。他们的方法揭示了模式与多余的体重。
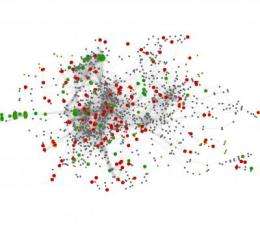
集合内的微生物人类肠道是一个繁忙的网络和能源使用的基因相互交错。通过构造模型微生物群落科学家发现,小说肥胖和苗条的人之间的区别。
他们能够检测组织转变远离正常肠道菌群的“精益”状态明显超重的人,以及在人炎症性肠病。研究结果发表在美国国家科学院院刊》上。
文章的资深作者,伊伯伦斯坦博士,华盛顿大学基因组科学助理教授,说,“我们的研究引入了一个新颖的框架,应用系统生物学和in-silico(计算机)建模研究人类微生物组的复杂整体微生物填充人体——作为一个有凝聚力的系统。”
莎朗Greenblum华盛顿大学的部门基因组科学和Peter j .恩伯FAS系统生物学中心的哈佛大学的研究小组。伯伦斯坦还持有一个兼职任命华盛顿大学的计算机科学与工程系,是外部圣菲研究所的教授。
团队的方法是将人类微生物组的凝聚力”supra-organism,”来自多个微生物物种的基因一致行动,好像他们是一个有机体的一部分。
伯伦斯坦说,全球研究项目,突出微生物如何影响人类健康。微生物对人类的发展至关重要,免疫力和营养。
人港口100万亿多个微生物。这些微生物生活在不同环境和人体解剖学中;肠道的房子最密集的人口,包含成百上千的细菌物种。他们的集体基因集合是巨大的:150倍人类基因的集合。
肠道微生物有助于保持我们的生命,制造维生素和蛋白质的基石,从食物中提取能量,赋予其抵抗疾病。先前的研究在肠道微生物,包括捐赠的微生物转移到接收方,表明操纵肠道菌群可能有用的临床应用。
“描述肠道微生物及其与人类宿主的相互作用有可能提供正常的人类生理学和疾病状态的深入见解,“Greenblum说,第一作者在纸上。
人类微生物组研究人员映射发现先前未知的物种和基因。基因研究确定不同物种的相对多度人类微生物组的某些人类物种的各种组合条件有关。研究人员已经观察到肥胖和苗条的人他们的肠道微生物组的差异。
初步结果是失踪,根据伯伦斯坦博士,是一个全面、系统级的了解这些微生物的基因构成的变化影响其组织,因此其代谢潜力(能源生产、使用和存储)及其对人类宿主的影响。
伯伦斯坦博士的研究小组获得的数据来自两个先前的研究描述的一组基因在肠道微生物组的精益和肥胖患者个人和炎症性肠病。
团队利用先进的计算技术重建模型的微生物群落和不同基因之间的相互作用。该组织还估计大量的酶的变化与各种主机相关的状态:瘦,肥胖,或与炎症性肠病的影响。
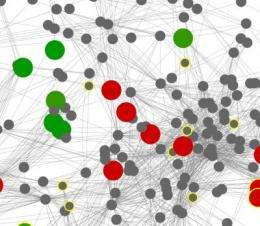
他们的模型反映代谢酶之间的相互依赖关系,而不是它们的物理位置在肠道。某些交互中心微生物群落的代谢。然而,这些酶典型肥胖或瘦大多远离核心网络及其关键代谢功能。这些酶在模拟网络的外围工作。这些外围酶代谢的第一步可能代表不依赖于物质生产的微生物或端点释放产品不使用的微生物,研究人员猜测。
伯伦斯坦解释说,这种酶可能会直接使用或生产物质描述肠道环境,并形成一个接口之间的微生物和人体的新陈代谢。
“我们的研究结果表明,enzyme-level变异与肥胖有关,炎症性肠病与变化的微生物与人类肠道环境如何相互作用,而不是微生物的核心代谢过程的变化,”伯伦斯坦说。
他说其他的发现指出,肥胖的微生物的潜在能力使用多样化的能源,这也许可以解释为他们增加从饮食中提取能量的能力。这种系统的方法可能也表明肥胖和炎症性肠病的生物标志物。标记可能表明常见的疾病或潜在的触发的反应肠道对疾病的微生物。
肥胖和苗条微生物网络模型之间的比较也显示,肥胖相关微生物水平较低的一个拓扑特征称为“模块化”。The reduced modularity of obese microbiome communities resembles that of single species that inhabit more constant environments.
虽然关联的研究可能不清楚地表明一个特定的机制复杂且知之甚少疾病,如肥胖和炎症性肠病、伯伦斯坦博士指出,他们展示的承诺用系统生物学的方法来研究人类微生物组及其对人类健康做出的贡献。
进一步探索