科学家在丙型肝炎病毒中找到了有前途的疫苗靶标
Scripps研究所的科学家领导的团队发现抗体可以预防细胞培养和动物模型中的丙型肝炎病毒(HCV)的广泛不同的抗体。
HCV非常高的突变通常有助于它逃避其主持人免疫系统。然而,新发现的抗体在很少突变的病毒包络处附着在位点上。其中一种新的抗体AR4a,显示比任何先前报道的抗HCV抗体更广泛的HCV中和活性。
斯克里普斯研究所的助理教授Mansun Law说:“这些抗体附着在以前未知的病毒包膜上,但现在是HCV疫苗的有希望的靶点。”劳是这份新报告的资深作者国家科学院的诉讼程序。
迫切需要一种有效的丙肝疫苗。的世界卫生组织(世卫组织)估计,病毒在全世界的130%至170万人中建立了大多数沉默感染 - 近3%的人口 - 每年蔓延到3至400万新人。HCV主要感染肝细胞,并被认为引起慢性,通常是无污染的肝脏炎症,最终可能导致严重的肝脏疾病。病毒已经负责大约四分之一的美国肝硬化和原发性肝癌病例,这是肝移植的主要原因。在一些发展中国家,HCV患病率极高;研究表明,在埃及,由于血液制品的筛查较差和注射器的重复使用,因此在埃及的人口中的多达22%是显而易见的。即使在发达国家,HCV感染也代表了迫在眉睫的公共卫生危机。在美国和欧洲,高达1400万人现在是HCV阳性,每年都有150,000人被新感染。
目前领先的丙型肝炎病毒感染治疗包括12- 36周的免疫刺激蛋白干扰素- α,抗病毒药物利巴韦林和丙型肝炎病毒蛋白酶阻断剂。但它并不是完全有效的,除了非常昂贵之外,还会引起严重的副作用。为了彻底消灭HCV大流行,特别是在发展中国家,科学家必须开发一种廉价的预防性疫苗。
然而,迄今为止有效的HCV疫苗是难以捉摸的。病毒突变非常迅速,因此,针对一个分离ate的HCV升高的抗体通常不会防止随后的HCV感染。HCV的医院样本表明,即使在个体患者内,病毒的基因和它们代码的蛋白质也是高度可变的。
“HCV疫苗开发的一个重要目标之一是在病毒中找到一个无法变化的病毒,”法律说。
为了找到这样的易感点,研究人员筛选了从感染者身上取样的抗体,寻找那些可以中和多种病毒株的抗体。这些具有广泛中和作用的抗体结合在病毒上的位置标记了脆弱的病毒结构,可作为广泛有效的抗体刺激疫苗的基础。之前的研究,包括2008年的一项研究自然医学,法律是牵头作者,发现了一些广泛中和HCV抗体。但对于目前的研究,法律和他的同事利用更彻底的方法,被称为“详尽平移”,看看他们是否可以找到新的甚至更广泛的抗体。“彻底的平移是一种强大的技术,用于寻找可能否则未被发现的罕见抗体,”法律说。
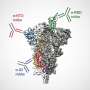
HCV采用两种包膜糖蛋白,E1和E2的复合物,抓住和熔断靶细胞。法律实验室的研究助理埃里克·普德收获了该病毒E1-E2复合物,在实验室中产生了HCV的细胞,并用作衍生自慢性HCV感染的人血液的抗体面板的“诱饵”。令人遗憾的淘汰技术涉及依次将该诱饵蛋白暴露于不同的抗HCV抗体,从而逐渐覆盖复合物上的已知抗体结合位点直到仅留下新的抗体。
以这种方式,Giang编剧了73个新的抗HCV抗体,其在E1-E2复合物上结合五个不同的“抗原区”。在HCV中和能力的标准细胞培养试验中,这些抗体中的几种表明通过各种HCV菌株中和感染的能力。一,AR4A,原来与E1-E2复合物上的几乎令人难度的斑点结合,靠近病毒外层脂肪分子的表面。AR4A显示出对测试面板中所有22个HCV菌株的显着中和能力 - 不仅在法律实验室的测试中,而且还在哥本哈根大学的确认测试中。
因此,新抗体比以前的顶部患有者AR3A更广泛地保护,他的2008年法律自然医学纸。“该人抗体AR4A具有本领域已知的最广泛的HCV中和活性,”法律说。
洛克菲勒大学合作研究人员,他最近设计了一系列HCV感染的小鼠,表明AR4A抗体保护这些小鼠免受两个广泛不同的HCV菌株。半剂量的Ar3a和Ar4a抗体的组合工作较少。
Law和他的同事下一步是开始制造和测试基于这些抗体研究中发现的脆弱的HCV结合位点的原型疫苗。研究人员还计划使用这种新的抗体来研究HCV蛋白的结构和功能,比如非常重要的E1-E2复合体。
抗HCV抗体如Ar4a和Ar3a也可以进行一些治疗用途。虽然他们将无法清除现有的HCV感染,但对大量人口来说是过于昂贵且难以使用的,以防止新感染,它们对于预防肝脏移植患者的新HCV肝脏感染可能是有用的。这种感染可以从患者体内的HCV储存器传播到新移植的肝组织。
“基于抗体的治疗方法非常适合肝脏移植到患者肝炎B病毒,我们希望新的HCV抗体对接受HCV肝移植的患者同样有帮助,”Law说。
进一步探索








用户评论