狗的新小脑性共济失调的基因识别
赫尔辛基大学的研究人员和Folkhalsan研究中心,芬兰,已经确定的遗传原因早发性进步小脑变性芬兰猎犬品种。汉斯·Lohi教授领导的研究中,发现一种新的疾病机制小脑变性。SEL1L基因突变被发现,没有以前的链接到遗传性小脑性共济失调。
这个基因发现第一犬早发性小脑变性,使基因测试的发展帮助根除疾病的品种。同时,SEL1L代表一种新的候选基因在人类早发性退行性共济失调。
这项研究发表在《科学》杂志上公共科学图书馆遗传学2012年6月14日。
遗传性共济失调影响人类和动物。人类的遗传性共济失调是一个异构的疾病,表现为小脑变性和功能障碍。小脑是大脑的一部分,参与协调运动。小脑结构的变性引起共济失调,这是一种神经缺陷的迹象可以影响步态运动协调,平衡,演讲和目光。大约20已知致病基因已确定在常染色体隐性和显性共济失调在人类但犬小脑性共济失调的遗传背景仍然是未知的。
芬兰猎犬小脑性共济失调的临床症状存在年龄的两个月。受影响的小狗有困难在控制他们的腿部运动,保持平衡。病程发展迅速,最后吃变得不可能,因为不受控制的头部动作。没有治愈疾病和影响幼犬必须安乐死。
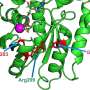
Lohi教授和同事们进行的这项研究显示小脑皮层的神经元损失影响芬兰猎犬小狗。通过比较基因组的影响和健康的狗,疾病的原因查明在SEL1L基因单核苷酸的变化。核苷酸变更引起编码氨基酸的改变SEL1L蛋白质。
“识别性共济失调的基因是第一个早发性退行性小脑性共济失调的基因已被确定在狗”,汉斯·Lohi教授说。除了芬兰猎犬,小脑变性已被确定在其他犬种。
“SEL1L基因没有被连接到小脑共济失调在任何物种,它代表了一种新的候选基因对人类早发性共济失调”,Lohi仍在继续。“事实上,我们已经筛选一小批人类患者可能的致病SEL1L突变”。
基因识别在芬兰猎犬揭示了一种新的疾病机制,这将有望进一步揭示神经元变性的发病机制。SEL1L达到进化保守的氨基酸变化功能域,并很有可能影响正常功能的蛋白质。SEL1L功能质量控制新合成的蛋白质,在细胞细胞器称为内质网。质量控制系统故障导致内质网压力最终导致细胞死亡。
“这是很有趣的,虽然SEL1L基因表达在几个不同的组织,我们只看到病变影响小脑皮层的狗。众所周知,小脑皮层的某些神经元内质网压力似乎非常敏感,这可能提供一些解释cerebellum-restricted细胞损失”,告诉M。Sc佳兆业集团Kyostila,文章的第一作者。“我们还可以测量增加内质网压力影响幼犬的小脑皮层,让更多的支持SEL1L致病基因在芬兰猎犬共济失调”,Kyostila补充道。
芬兰猎犬共济失调是一种单基因缺陷,在常染色体隐性遗传方式。据调查,有10%的芬兰猎犬携带隐性共济失调的基因突变。基因测试已经开发了繁殖的目的。测试使得识别疾病携带者,并与非承运人交配时,他们也可用于育种程序。如果所有的载体狗被育种者排除在外,品种的遗传多样性可能会受到影响。芬兰猎犬共济失调dna测试实验室提供的测试是Genoscoper (genoscoper.com),并是第一个测试本机芬兰研究小组开发的品种。
进一步探索