科学家发现生物机制可以引发癫痫发作
科学家们发现了第一个直接证据,证明长期以来被怀疑在癫痫中存在的一种生物机制能够引发大脑癫痫发作,这为寻求改进治疗方法甚至预防性治疗的研究打开了大门。
辛辛那提儿童医院医疗中心的研究人员9月19日报告神经元这种被称为颗粒细胞的小神经元(位于大脑齿状回区域)的分子破坏,导致小鼠的大脑癫痫发作,与人类的癫痫发作相似颞叶癫痫.
齿状回位于海马体的颞叶颞叶癫痫是这种疾病最常见的形式之一。
“癫痫是一种罕见的疾病,我们没有真正的预防性治疗方法,目前的诊断后治疗可能有严重的副作用,”辛辛那提儿童麻醉科的神经科学家、该研究的首席研究员史蒂文·丹泽博士说。“确定哪些细胞和机制负责癫痫发作,使我们能够开始研究如何以更精确的方式控制或消除这一问题。”
癫痫可由多种原因引起,包括扰乱正常大脑发育的儿童出生缺陷。脑损伤严重的儿童和成人也会出现这种症状。丹泽说,这些人可能有很高的风险患上某种形式的癫痫,这取决于他们受伤的位置和严重程度。
基因改变的技术进步实验室的老鼠模拟人类疾病使得科学家们有可能在齿状回颗粒细胞(DGCs)中产生特定分子破坏的动物。DGCs是仅有的两个种群之一神经细胞在另一个人的成熟大脑中继续大量形成嗅觉神经元.这是有益的考虑海马体负责学习和记忆齿状回是大脑中兴奋性信号的大门,如果调节不当,可能会导致癫痫发作。
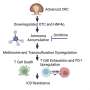
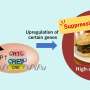
几十年来,人们一直观察到异常DGCs在癫痫中的存在,尽管在目前的研究之前,缺乏将其与癫痫发作联系起来的证据。Danzer和他的同事能够从小鼠出生后形成的DGCs中删除一种名为PTEN的基因。这导致了一种称为mTOR(雷帕霉素的哺乳动物靶标)的分子途径的过度激活,这种分子途径调节细胞生长,在某些情况下过度激活时也与肿瘤形成和癌症有关。
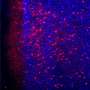
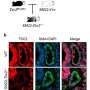
在Danzer和他的同事的测试中,mTOR的过度激活导致小鼠的DGCs之间产生异常的神经连接——类似于在人类颞叶癫痫中观察到的情况——并且动物经历了癫痫发作。即使在DGC总数中PTEN基因缺失的比例不到10%的小鼠中,异常的神经连接和癫痫也会发生,这加强了DGC的生物学破坏和癫痫之间的联系。
当研究人员用一种阻断mTOR通路的药物——雷帕霉素治疗癫痫小鼠时,癫痫停止了,并巩固了与PTEN-mTOR通路的联系。在辛辛那提儿童医院(Cincinnati Children’s),雷帕霉素在治疗结节性硬化症(结节性硬化症是一种良性但仍然危险的肿瘤,可在关键器官周围形成)方面的试验已经成功。有趣的是,患有结节性硬化症的人也有患癫痫的风险,Danzer说。辛辛那提儿童医院(Cincinnati Children’s)也在测试新型mTOR抑制剂治疗癫痫。
丹泽正在跟进目前的研究,试图从已经患有癫痫的老鼠的大脑中消除异常的DGCs,并观察这是否会阻止癫痫发作。研究人员正在尝试用白喉毒素系统性地治疗小鼠。
虽然白喉毒素通常对小鼠细胞没有毒性,但在他们的实验中,研究人员将在异常的小鼠DGCs中添加一种分子,与毒素结合。理论上,这应该能让毒素杀死异常的dgc。如果治疗停止癫痫发作Danzer说,该研究将进一步验证异常DGCs与癫痫发作之间的联系。这也将允许研究人员开始对治疗和预防的前瞻性治疗策略进行实验室测试。
涉及PTEN和mTOR通路的突变也在其他神经疾病中被发现,如自闭症和精神分裂症。丹泽说,目前的研究结果可能会吸引研究这些疾病和其他涉及出生后产生的异常颗粒神经元的研究人员的兴趣。
Danzer说:“在少量颗粒细胞中破坏这一途径的深远影响表明,齿状细胞可能是其他神经疾病中mTOR途径突变的关键靶点。”“我们相信神经系统科学家我们会对颗粒细胞破坏对神经系统的巨大影响感到惊讶,并对一种潜在的新型疾病机制的展示感兴趣。”