组蛋白突变在儿童脑癌发病机制的研究
(欧宝娱乐地址医学快报)大多数癌症治疗都是钝性的。为了根除肿瘤,肿瘤学家通常采用放疗或化疗,这可能会在癌细胞生长的同时损害健康组织。洛克菲勒大学C. David Allis实验室的新研究可能会让科学家们更接近于设计出能够精确定位肿瘤的癌症治疗方法。
他们的研究结果今天在网上发表科学快讯在此之前,几位国际科学家最近也有了一系列的发现基因组测序财团直接链接突变组蛋白蛋白质一种罕见的儿童脑干癌叫做DIPG。总的来说,这些研究代表了科学家第一次将组蛋白突变与疾病联系起来,并引起了彼得·刘易斯的兴趣,他是艾丽斯染色质生物学和表观遗传学实验室的研究助理,他是这些新研究的先锋。
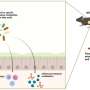
组蛋白与DNA一起组成基因包装材料称为染色质。该突变发生在组蛋白H3上,涉及到组蛋白尾部关键位置的一种氨基酸(蛋氨酸)与另一种氨基酸(赖氨酸)的显著特异性替代,“沉默”了相关基因。通常情况下,当一种名为甲基转移酶的酶(包含一个名为SET结构域的结构区域)将一个甲基化学基团附着在H3尾部27号位置的赖氨酸上时,基因沉默就会发生。这种高度特异性的化学反应,被称为甲基化,被蛋氨酸取代赖氨酸所破坏,这可能导致基因调控错误。
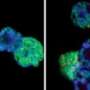
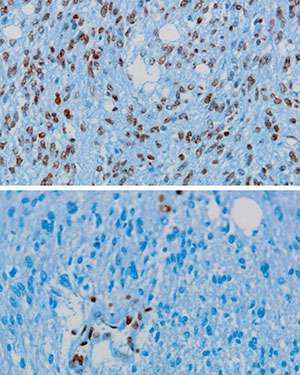
Lewis和他的同事研究了含有蛋氨酸到赖氨酸替代的人类DIPG肿瘤,并确定突变的组蛋白H3占DIPG样本中总H3的3.6%到17.6%。他们还发现,当少量突变H3添加到正常H3组蛋白中时,正常H3组蛋白的甲基化水平整体下降人类细胞.
“我经常说,‘组蛋白中的每个氨基酸都很重要,’”乔伊和杰克·菲什曼教授艾利斯说。“这些研究强调了这可能是多么正确。”
研究人员继续证明,正常H3组蛋白甲基化的减少是由于干扰a甲基转移酶被突变组蛋白称为PRC2。PRC2对正常H3的甲基化导致参与细胞生长途径的基因受到抑制。如果没有甲基化,参与这些途径的基因可能会被激活,促进DIPG中肿瘤的生长。Allis和Lewis接受了美国国立卫生研究院和斯塔尔癌症协会的资助。这项工作的主要合作者包括杜克大学医学中心的Oren Becher和普林斯顿大学的Tom Muir及其同事。
“我们的发现为我们探究生物过程提供了一个有用的工具,”刘易斯说。“这也告诉我们如何抑制酶,这可能会导致模仿这些突变体作用的药物的开发。”
“我们现在有了一个通过突变组蛋白抑制PRC2的异常表观遗传沉默来促进脑干癌的模型,”Allis说。“我们已经发现了一种潜在的有用机制,可以专门抑制单个set结构域甲基转移酶,以及可能涉及各种恶性肿瘤的其他染色质修饰酶。”
进一步探索