重新发明药物发现:对ALS的有希望的药物目标
利用一种新的基于干细胞的药物筛选技术,这种技术有可能彻底改造并大大降低新药物开发的成本,哈佛干细胞研究所(HSCI)的研究人员发现,一种化合物在保护肌萎缩性脊髓侧索硬化症(ALS)中死亡的神经元方面比两种在人类临床试验中失败的药物更有效,这两种药物已经投入了数亿美元。
新的干细胞筛选技术由李鲁宾,哈尔维尔执行委员会成员和哈佛干细胞系和再生生物系教授开发,成功预测,这两种药物最终失败的人类测试的第三阶段也会失败。
“这是药物发现的深刻,黑暗的秘诀,即在人类中已经测试了很少有药物 -患病细胞在活人身上进行测试之前,”HSCI转化医学项目负责人鲁宾说。
“我们对我们可以使用的概念感兴趣干细胞来纠正这种情况。”
Rubin的模型建立在由HSCI首席教师Kevin Eggan开发的早期概念上,据证明,可以使用携带患者患者基因的干细胞将基于神经元的疾病移动到实验室菜中。
在今天发表的论文中细胞干细胞,鲁宾列出了他和他的同事如何应用他们基于干细胞的新方法药物发现肌萎缩性侧索硬化症。这种疾病与运动神经元的逐渐死亡有关,运动神经元在大脑和肌肉之间传递信息。随着细胞的死亡,肌萎缩性侧索硬化症患者会经历四肢无力,然后迅速瘫痪呼吸衰竭。这种疾病通常在生活中稍后罢工。10%的病例是遗传倾斜的,但对于大多数患者而言,没有已知的触发器。
鲁宾的实验室首先在老鼠身上研究这种疾病,从老鼠胚胎干细胞中培育出数十亿运动神经元,其中一半正常,另一半有已知导致ALS的基因突变。
研究人员让这些细胞缺乏营养物质,然后筛选5000个类似药物的分子,以找到能让运动神经元存活的分子。
鉴定了几次命中,但最佳延长正常和Als电机神经元的寿命的分子是Kenpaullone,以便抑制酶(GSK-3)的作用,该酶(GSK-3)接通和脱离几种细胞过程,包括细胞生长和死亡。“令人震惊地,该分子使细胞保持比标准培养基更好地保持每个人都能使电动神经元保持在内,”鲁宾说。
Kenpaullone在几个后续实验中证明有效,使小鼠电机神经元在某些死亡的情况下。神经元存活在分子存在下增加细胞是否被编程为死或置于有毒环境中。
经过进一步的研究,鲁宾的实验室发现,肯波隆的效力来自于它也能抑制HGK——一种酶,它能引发一系列反应,导致运动神经元死亡。这种酶以前并不知道它在运动神经元中有重要作用,也不知道它与肌萎缩性侧索硬化症有关,这标志着发现了治疗该疾病的新药物靶点。
“我认为干细胞屏幕将发现以前从未发现过的新化合物,”鲁宾说。“我很高兴能够认为有一天他们的一个可能真的足够好进入诊所。”
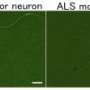
要了解kenpaullone在患病人体细胞中的作用,鲁宾的实验室暴露于从人胚胎细胞生长到分子的患者电机神经元和运动神经元,以及两种在小鼠中均未良好的药物,但在ALS的III期人类临床试验中失败。再一次,Kenpaullone增加了神经元生存率的速度,而一种药物看到的反应很小,而其他药物未能保持任何细胞活着。
根据鲁宾的说法,在Kenpaullone可以用作药物之前,它需要一个大量的分子化妆,使其能够更好地靶向细胞并找到它进入脊髓的方式,以便进入脊髓运动神经元。
“这在某种程度上证明了整件事的可行性,”他说。“我认为使用这种方法来发现新的药物靶点和对真实人类疾病的化合物进行预验证是有可能的细胞在把他们送到诊所之前。”
与此同时,鲁宾的下一步将是继续寻找更好的类药物化合物,以抑制HGK,从而提高运动神经元的存活率。他认为,这项研究得出的新信息将对学术界和制药行业有用。
鲁宾说:“这种探索性的筛选很难获得资金支持,所以成为HSCI的一部分是绝对必要的。”HSCI提供了部分资金。
进一步探索












用户评论