新分子途径的异常可能会增加乳腺癌的风险
据发布在乳腺癌患者中,已经确定了涉及基因ZnF365基因的新分子途径,并且该途径异常可能会预测乳腺癌患者的预后较差。癌症发现,美国癌症研究协会杂志。
“基因组不稳定性是增加的趋势异常变化在DNA中,就像添加染色体的额外副本一样,DNA断裂和突变,”纽约州威尔·康奈尔医学院病理学和实验室医学系助理教授Ji-Hye Paik博士说:“因为这些遗传异常增加了发展肿瘤的机会,所以它是从根本上重要的是了解预后和治疗中癌症基因组不稳定性的分子基础。”
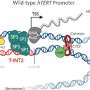
端粒是保护染色体免受恶化的染色体末端的片段。随着端粒的长度缩短,它们激活了细胞死亡,由肿瘤抑制基因,p53。这个过程对于抑制癌症至关重要,功能失调的端粒会导致染色体异常和癌症。
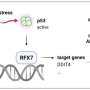
Paik及其同事使用设计为易受癌症的细胞,证明p53激活了ZnF365以维持基因组稳定性。研究人员发现,缺乏ZnF365的细胞显示出DNA不完全加倍的迹象,从而导致异常细胞分裂和不等的染色体。他们得出的结论是,由于ZnF365促进了细胞分裂的及时分辨率,因此其损失导致异常数量的染色体,称为非整倍性,这与包括癌症在内的许多疾病有关。
“我们的研究是第一个证明分子机制p53 – ZNF365 -TELOMERE途径的基础,并显示该途径中的变化如何导致增加癌症风险,”帕克说。“了解这一途径为癌症提供了新的治疗机会。”
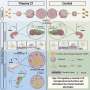
为了了解ZnF365在癌症中的作用,Paik和同事使用了癌症基因组图集(TCGA)可用的数据,并分析了49种三重阴性乳腺癌(TNBC)中Znf365的表达 - 最积极的形式乳腺癌- 和300个非TNBC。他们发现ZnF365的表达在TNBC中最低,并且在非TNBC中仍然很高。
研究人员使用来自TCGA的2,978名妇女的较大队列的数据,还发现,在拥有10年无复发生存的女性中,ZnF365表达高的女性的生存优势提高了26%。此外,当研究人员分析在包含18种正常乳腺组织,141个TNBC和145个非TNBC的组织微阵列中存在ZnF365时,正常乳腺组织和非TNBC中存在ZnF365,但在TNBC中的表达下降了。
根据Paik的说法,这项研究是第一个确定ZnF365在不同类型的乳腺癌中表达的研究,并且由于它预测了疾病的预后,因此ZnF365可能是患者分层的潜在生物标志物。
进一步探索