未能摧毁有毒蛋白质 - 没有蛋白质本身的堆积 - 促成亨廷顿的疾病
阿尔茨海默,亨廷顿,帕金森。名称永远与他们所代表的内容相关联:毒害大脑神经元并将整个地区枯竭并死亡。这些和其他所谓的神经变性疾病通常与导致神经元死亡的有毒蛋白质的累积有关。但是现在,Gladstone机构的科学家发现,疾病的进展不是由于毒素本身的积累,而是在个体神经元的能力冲洗这些毒素的能力。此外,它们鉴定了可以提高这种能力的治疗靶,从而保护大脑免受疾病的致命作用。
在最新问题中自然化学生物学,Gladstone调查员Steve Finkbeiner实验室的研究人员描述了博士,描述了新开发的技术如何让他们第一次看到,单个神经元如何随着时间的推移反对毒性蛋白质的积聚。该团队将其努力致力于亨廷顿疾病的模型,观察了大脑中不同类型的神经元有何反应,每个毒性累积具有不同程度的成功,提供了为什么该疾病在一个区域中导致神经元死亡的线索,而神经元在另一个人的污染。
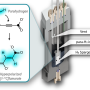
“亨廷顿 - 一种遗传和致命的疾病,导致肌肉协调,认知和个性的问题 - 以突变形式的毒性累积为特征亨廷顿蛋白在大脑中,“Finkbeiner博士解释为Gladstone指导Taube-Koret疾病研究中的神经退行性疾病研究。Finkbein博士也是一位教授神经病学加州大学旧金山大学的生理学,Gladstone都是附属的。“研究人员之间的长期谜团是突变亨廷顿蛋白的积累是如何引起细胞降解和死亡的,但之前的技术使得几乎不可能看到和监控这个过程细胞水平。在这项研究中,我们采用了一种称为光学脉冲标记或OPL的方法,使我们能够看到突变的亨廷特如何通过神经元随着时间的神经元蹂躏大脑。“
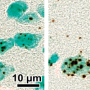
使用从亨廷顿的啮齿动物模型中提取的神经元,该团队使用了OPL方法,该方法监测了不同类型的神经元能够冲出突变亨廷顿的速度和效率。细胞可以清除毒素的速度越快,神经元幸存的时间越长,反之亦然。
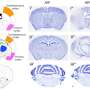
令人惊讶的是,研究团队注意到不同类型神经元对澄清突变亨廷顿的能力的明显差异。位于纹章中的神经元 - 主要受亨廷顿疾病影响的大脑区域,这些疾病涉及肌肉运动 - 特别易受。在其他地区发现的神经元,例如皮质和小脑,较少。当他们跟踪携带突变亨廷特的纹状体神经元时,它们发现它们比来自其他大脑地区的人更容易死亡。
所有细胞都依赖于两种主要方法,以清除过量的蛋白质:泛素 - 蛋白酶体系(UPS)和自噬。虽然它们的机制是截然不同的,但它们的目标是相同的:从字面上吞噬过量的蛋白质,确保它们有效地冲洗,以便不干扰正常的细胞活性。
研究小组发现,纹状体神经元对自噬过程中断特别敏感。但球队在解决这个问题方面找到了一种方法。它们通过促进这些神经元中叫做NRF2的蛋白质的活性来人为地加速自噬,该蛋白质延长了细胞存活。
“如果我们可以制定促进NRF2生产的药物神经元最容易受到亨廷顿的影响,我们可能会延长他们的生存,从而履行疾病的最严重影响,“前格拉德斯通博士博士博士,博士,该研究的主要作者。”重要的是,我们的结果也表明大脑本身已经发展起来亨廷顿等疾病的强大应对机制。例如,人们不会开始在他们生命的第四或第五十年中开始经历亨廷顿的症状 - 尽管突变亨廷顿在出生时存在 - 进一步证明大脑避免疾病影响的能力。“
“我们的调查结果对于向我们通知我们对亨廷顿等疾病的潜在机制至关重要,也提醒研究人员仅关注造成疾病的蛋白质 - 而不是单个细胞如何应对IT - 只是一方铸币,“Finkbein博士说。“真正了解像亨廷顿这样的复杂疾病,我们也必须展望大脑的自然进化的防御机制,因为我们在这里表现出来可能代表一个完全新的治疗策略。”
进一步探索










用户评论