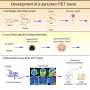
关键分子途径导致阿尔茨海默氏症
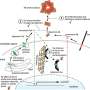
关键的分子途径,最终导致晚发性阿尔茨海默病,最常见的障碍,发现了哥伦比亚大学医学中心的研究人员(CUMC)。研究,结合系统生物学和细胞生物学工具,提出了一种新的阿尔茨海默病研究的方法,着重分析了几种新的潜在的药物靶点。今天的论文发表在杂志上自然。
了解阿尔茨海默氏症的大部分来自实验室的研究少见,早发性、家庭(继承)形式的疾病。“等研究提供了重要线索潜在疾病的过程,但是目前还不清楚这些罕见的家庭形式的阿尔茨海默氏症与常见的疾病,”研究带头人Asa Abeliovich说,医学博士,博士,副教授的病理学和细胞生物学陶布研究所的神经学研究阿尔茨海默病和CUMC衰老的大脑。“最重要的是,许多药物‘工作’在家族性疾病的小鼠模型最终失败了在晚发性阿尔茨海默氏症患者进行测试。这使得我们和其他实验室、追求机制常见的疾病。”
Non-familial阿尔茨海默氏症是复杂的;它被认为是由遗传和环境危险因素的组合,每个单独有适度的影响。使用所谓的全基因组关联研究(GWAS),之前的报告已经确定了几个常见的基因变异,增加老年痴呆症的可能性。一个关键目标是了解这些常见的遗传变异函数影响阿尔茨海默氏症的可能性。
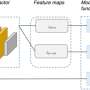
在当前的研究中,CUMC研究者确认键分子通路该链接等遗传风险因子阿尔茨海默氏症。工作结合细胞生物学和系统生物学研究工具,基于复杂网络的计算分析基因的表达变化的风险人类的大脑。
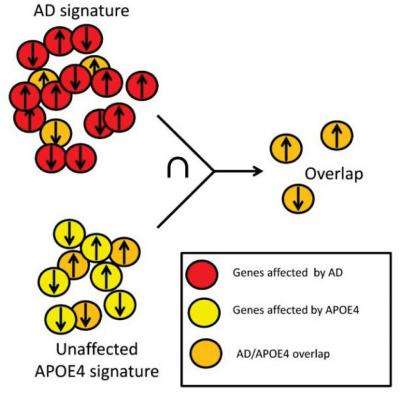
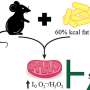
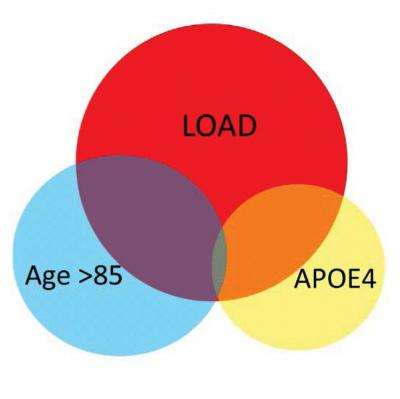
更具体地说,研究人员首先专注于最重要的遗传因素,这将对阿尔茨海默氏症高危人群,APOE4(发现在大约三分之一的个人)。有一份这种基因变异的人,发展成晚发型阿尔茨海默氏症的风险增加3倍,而那些有两个副本十倍增加的风险。Abeliovich博士说:“在这项研究中,“我们最初问道:如果我们观察脑组织解剖从阿尔茨海默氏症的高危个体,有一致的模式吗?”
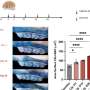
令人惊讶的是,即使在没有阿尔茨海默病的情况下,脑组织从高危个体(他们进行APOE4基因)存在一定的变化让人想起那些成熟的阿尔茨海默氏症,”Abeliovich博士说。“我们因此集中在试图了解这些变化,这似乎使人们处于危险中。大脑的变化,我们认为是基于“转录组”——广泛的分子成千上万个基因的表达水平的调查中表达的大脑。”
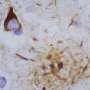
使用上面提到的网络分析工具,研究人员又发现了一个打候选人“主调节器”因素,链接APOE4的级联破坏性的事件,在阿尔茨海默氏痴呆的高潮。随后的细胞生物学研究表明,许多这些主监管机构参与处理和贩卖大脑神经元内淀粉样前体蛋白(APP)。应用程序产生β淀粉样蛋白,蛋白质积累在老年痴呆症患者的大脑细胞。总之,工作最终连接这些点之间的一种常见的遗传因子,将阿尔茨海默氏症的高危个体,APOE4,疾病病理。
在确定的候选人“主监管机构”,团队进一步分析两个基因,SV2A RFN219。“我们SV2A特别感兴趣,因为它的目标是常用的抗癫痫药物,levetiracetam。这个建议的治疗策略。但还需要更多的研究才能发展的临床试验患者levetiracetam晚发性阿尔茨海默病的迹象。”
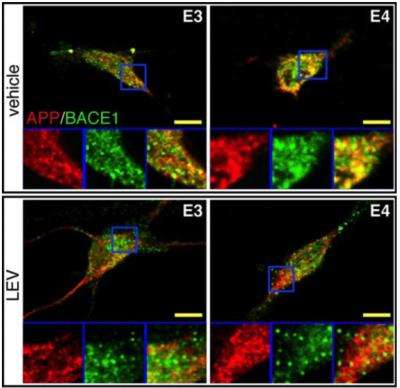
研究者使用人为评估SV2A的作用,神经元APOE4基因变异。(直接转换生成的神经元的皮肤成纤维细胞为阿尔茨海默氏症高危个体,使用Abeliovich实验室开发的技术)。治疗神经元港APOE4高危基因变异与levetiracetam(抑制SV2A)导致减少β淀粉样蛋白的生产。研究还表明,RFN219似乎扮演一个角色在APP-processing有APOE4变异的细胞。
“我们的发现表明SV2A和RFN219都是候选人药物靶点”Abeliovich博士说。“令我们兴奋的是,这些方法可能在药物的开发中发挥作用的共同non-familial形式阿尔茨海默氏症疾病。这是一个巨大的挑战。”
更多信息:自然DOI: 10.1038 / nature12415