对神经元回路控制的新见解可能导致遗传性运动障碍的治疗
小脑是大脑的一个地区,对平衡,学习运动技能和运动的协调。在小脑的外层中,个体'purkinje'细胞从脑干的输入和成千上万的颗粒细胞集成,以产生小脑'输出'。Purkinje细胞和相关平行纤维之间的连接对适当的小脑功能至关重要,但是关于底层的分子机制是非常少的。
来自Wako riken脑科学研究所的Katsuhiko Mikoshiba的一支由Katsuhiko Mikoshiba领导的研究人员现在已经确定了负责维持这些的完整性的信号分子神经元电路在成熟的小脑。
1型肌醇三磷酸受体(IP3.R1)已知在浦肯野细胞中高水平表达。IP的突变3.R1基因导致不协调的运动,异常的Purkinje细胞结构和小鼠中豚细胞和平行纤维之间的信号传导,并导致人类疾病称为纺纱脑共济失调15(SCA15)。MikoShiba和他的同事调查了知识产权的作用3.R1在成熟小脑中通过基因工程小鼠在浦肯野细胞中缺乏受体。
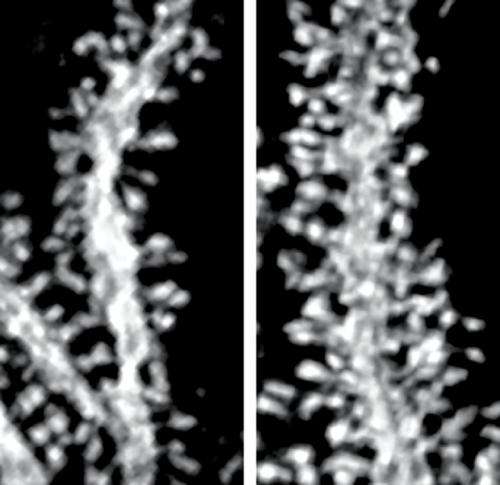
研究人员发现突变小鼠表现出运动技能学习障碍和严重的不协调运动或共济失调,如在sc15患者中所见。在显微镜下仔细观察小脑也发现了小鼠浦肯野细胞的异常。而出现的正常发育,成年动物细胞表现出显著增加其树突spines-the微小卫星传回的密度和长度与其他细胞突起形成连接(图1)。所有的刺,不过,形成全功能连接平行在成年动物纤维。
之前,Mikoshiba的团队展示了IP3.R1在突触可塑性过程中起着关键作用,神经元之间的连接在学习过程中增强或减弱。这些新发现表明,该受体也是维持成人小脑连接的适当空间安排所必需的。
“老鼠缺乏知识产权3.R1专门在Purkinje细胞显示共济失调类似于SCA15患者,“Mikoshiba说。他指出,自浦本细胞的异常维持以来树突棘似乎与突变小鼠的严重共济失调有关,小脑回路的维持缺陷可能同样参与了sc15的发病机制。
“我们现在正在研究如何IP的精确机制3.R1调节浦肯野细胞脊柱维持。这可能阐明了sc15的发病机制,并导致新疗法的发展,”Mikoshiba补充说。
进一步探索













用户评论