细菌尾部含有肠道炎症
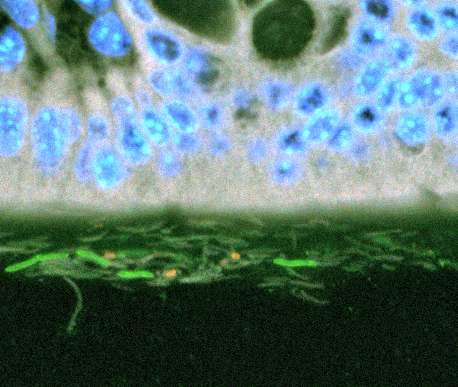
在健康的个体中,人类肠道的内衬与胃肠道中大约100万亿个细菌细胞的唯一区别是一层黏液层。
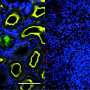
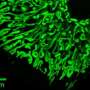
但当肠道细菌与细胞接触肠道的表面,炎症由细菌细胞蛋白质引起的。一种特别有效的蛋白质来自推动微生物的细菌螺旋状尾巴。虽然一些最丰富的细菌在肠道中使用这些尾巴(鞭毛)推进,但健康的肠道中引起炎症的蛋白质(鞭毛蛋白)的水平非常低。这意味着必须有某种控制机制来限制它们的生产。
现在,康奈尔大学领导的一项研究发表在11月13日的杂志上细胞宿主和微生物揭示了肠道细菌和免疫系统之间复杂的动态关系,而免疫系统确实控制着鞭毛蛋白。
这项研究由美国国立卫生研究院、哈特韦尔基金会、阿诺德和梅布尔·贝克曼基金会以及露西尔和戴维·帕卡德基金会资助。
“肠道泵出了六至10克抗体的抗体,”微生物学助理教授和研究的高级作者露丝·莱里说。Ley实验室的研究生Tyler Cullender是本文的第一作者。
由免疫系统产生的抗体,附着于异物。在肠道中,称为IgA的抗体特异性涉及鞭毛蛋白。抗体像胶水一样,产生粘液层,将细菌与肠道分开,说Ley。
但是,“被粘合的细菌不是愚蠢的,”莱伊说。“一旦他们感觉到抗体 - 或者他们被困 - 他们停止制作鞭毛,这可能会限制他们在粘糊糊的层中游泳的距离,说谎。较少的鞭毛蛋白蛋白与肠衬有关,炎症较少。
研究人员研究了缺乏称为TLR5的受体的小鼠,用于检测鞭毛蛋白蛋白。如果没有检测器,这些小鼠在鞭毛蛋白存在下未能产生足够的IgA抗体。没有抗体,许多肠道细菌开发了鞭毛并靠着肠道的细胞。
当Ley和他的同事们去除这些老鼠的肠道细菌,并添加抗体在实验室中,细菌停止生产鞭毛。“它努力固定他们,”莱伊说。
研究人员的下一步是确认鞭毛蛋白接近肠道黏膜会引发炎症,从而引发代谢性疾病。事实上,没有TLR5受体的小鼠会出现代谢综合征,这是一种伴随一系列疾病的疾病,包括血压升高,高血糖,多余的腰体脂肪和异常的胆固醇水平,这种胆固醇水平一起发生并增加心脏病,中风和糖尿病的风险。Ley和同事曾先前表明过gut microbiota.小鼠需要进行这些症状,并且进一步研究是为了表明细菌游泳是推动疾病的关键。
进一步探索









用户评论