Rock和Rho:帮助癌细胞前进的蛋白质
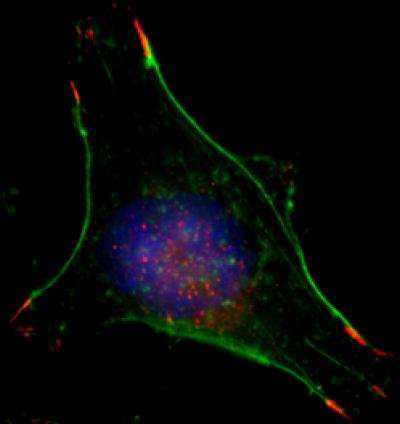
约翰·霍普金斯大学(Johns Hopkins University)的生物学家发现,肿瘤内部经常持续的低氧条件足以启动分子链事件,将乳腺癌细胞从僵硬的静止状态转变为可移动的侵袭性细胞。他们的证据发表在美国国家科学院院刊12月9日,强调了缺氧诱导因子在促进乳腺癌转移中的重要性。
高水平的RhoA和ROCK1已知会恶化预后乳腺癌患者通过赋予癌细胞移动的能力,但它们产生的触发器是一个谜,”Gregg Semenza,医学博士,约翰霍普金斯大学医学院的C. Michael Armstrong医学教授和这篇文章的高级作者说。“我们现在知道,当乳腺癌细胞暴露在低氧环境中。”
Semenza说,为了移动,癌细胞必须改变其内部结构。细细的、平行的细丝遍布整个细胞,使它们能够收缩,细胞的“手”就会升起,使细胞能够“抓住”外部表面来拉自己。已知蛋白质RhoA和ROCK1是这些结构形成的中心。
此外,编码RhoA和ROCK1的基因已知在高水平上被打开人类细胞转移性乳腺癌。在少数情况下,这些水平的升高可以追溯到一种控制蛋白质的基因错误,但在大多数情况下并非如此。Semenza说,这项活动促使他和他的团队寻找导致蛋白质水平高的另一个原因。
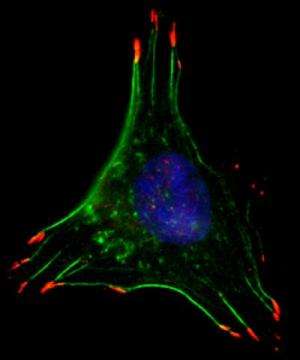
研究表明,乳腺癌中经常出现的低氧条件,通过缺氧诱导因子的作用,成为了增加RhoA和ROCK1生成的触发器。
Semenza解释说:“随着肿瘤细胞的繁殖,肿瘤内部的氧气开始耗尽,因为它没有得到血管的供给。”“缺氧会激活缺氧诱导因子,这是一种主控蛋白,能启动许多基因,帮助细胞适应缺氧。”他解释说,虽然这些反应对生命至关重要,但缺氧诱导因子也会启动基因,帮助癌细胞通过入侵血管逃离缺氧肿瘤,并通过血管扩散到身体的其他部位。
Daniele Gilkes博士是一名博士后,也是该报告的主要作者,她分析了人类转移性乳腺癌在实验室低氧条件下生长的细胞。她发现,与生理正常水平相比,细胞在低氧状态下的流动性更强。每个细胞有三倍的纤维和更多的“手”。然而,当缺氧诱导因子蛋白质水平被降低时肿瘤细胞几乎没有动过。细胞内纤维和“手”的数量和收缩能力也有所下降。
当吉尔克斯测量RhoA和ROCK1蛋白质的水平时,她发现在低浓度环境中生长的细胞中,这两种蛋白质的水平都有很大的增加氧气.然而,当对乳腺癌细胞进行修饰以降低缺氧诱导因子的数量时,RhoA和ROCK1的水平降低了,表明这两组蛋白质之间有直接的关系。进一步的实验证实,缺氧诱导因子实际上与RhoA和ROCK1基因结合,使它们启动。
然后,该团队利用一个数据库,让他们可以询问在乳房中是否开启了RhoA和ROCK1基因癌症细胞影响患者的生存。他们发现,RhoA或ROCK1蛋白水平高的女性,尤其是这两种蛋白水平都高的女性,死于乳腺癌的可能性比RhoA或ROCK1蛋白水平低的女性高得多。
“我们已经成功地降低了流动性乳腺癌细胞在实验室中使用基因技巧来降低缺氧诱导因子,”吉尔克斯说。“现在我们了解了其中的机制,我们希望进行临床试验,以测试抑制缺氧诱导因子的药物是否具有阻断RhoA和ROCK1的产生和防止乳腺癌妇女转移的双重效果。”
进一步探索