科学家发现了应激线粒体的新的生存机制
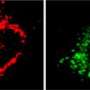
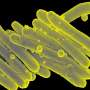
斯克里普斯研究所(TSRI)的科学家们发现了细胞用来保护线粒体的一种自然机制,线粒体是一种微小但必不可少的“发电厂”,为全身细胞提供化学能量。线粒体损伤被认为是常见神经退行性疾病、癌症甚至衰老过程的一个重要因素。TSRI研究人员的发现可能会导致保护线粒体免受这种损伤的新方法,从而改善人类健康。
TSRI分子与实验医学系Arlene and Arnold Goldstein助理教授R. Luke Wiseman说:“我们发现的机制可能为我们治疗许多涉及线粒体功能障碍的疾病提供了另一种方法。”
怀斯曼是这项新研究的资深作者,该研究发表在2013年12月3日的杂志上细胞代谢.
细胞的发电厂
线粒体是一种微型反应堆,它燃烧氧气来制造ATP, ATP是细胞的基本单位化学能在细胞。因此,它们是我们呼吸氧气的主要消费者。
但是氧分子集中在里面线粒体是高度反应性的,倾向于以不想要的方式修饰蛋白质,将它们改变成异常形状,并经常导致它们变得功能失调和聚集在一起。如果这种错误折叠和聚集失控——由基因突变、衰老和环境毒素(如农药)等因素引起——结果可能是线粒体失效和细胞死亡。
为了保护自己免受过多蛋白质的错误折叠和聚集,细胞进化出了在压力下保护线粒体的信号通路。这些途径主要通过增加线粒体“伴侣”分子的产生来发挥作用,这些分子有助于保持线粒体内蛋白质的正确折叠,以及蛋白酶的产生,蛋白酶可以切割错误折叠和聚集的线粒体蛋白质。
怀斯曼说:“到目前为止,在哺乳动物细胞中,这些调节线粒体‘蛋白质平衡’机制的信号通路的特征还很模糊,但总的来说,它们似乎对细胞在压力下的生存非常重要。”
减轻负担
在这项新研究中,Wiseman和他的实验室成员,包括第一作者Kelly Rainbolt和Neli Atanassova,专注于线粒体蛋白质平衡调节的第三种机制:减少蛋白质“输入”线粒体。
Rainbolt说:“我们预测,减少进入线粒体的新输入蛋白质的数量将减少细胞应激期间线粒体伴侣和蛋白酶的负担。”
研究小组首先研究了一种名为TIM23的蛋白质复合物,它是蛋白质进入线粒体内部部分(或基质)的主要进口商之一。TIM23包含一个名为Tim17的核心亚基,在哺乳动物中是独一无二的,它有两个几乎相同的变体,Tim17A和Tim17B,它们合并成不同的复合物。研究人员使用一种环境毒素亚砷酸盐,在培养的哺乳动物细胞中诱导一般的应激反应,并监测Tim17A和Tim17B的变化。
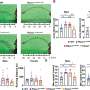
结果显示,细胞线粒体中的Tim17A水平在亚砷酸盐的作用下急剧下降,而Tim17B水平则不受影响。有趣的是,作者发现Tim17A的减少是由一个已建立的生物信号通路下游诱导的细胞在压力。Tim17A的减少不仅是因为Tim17A的产量减少,还因为Tim17A的降解速度比通常更快。研究小组很快发现,一种线粒体蛋白酶YME1L负责应激诱导的Tim17A降解。
Rainbolt说:“已经建立的保护性生物信号通路诱导Tim17A降解的能力向我们表明,Tim17A降解可能是一种保护机制,可以促进线粒体蛋白平衡以应对病理损伤。”
事实上,科学家们证明,减少Tim17A蛋白水平可以增加细胞存活率,以应对直接挑战线粒体蛋白质平衡和功能的压力。
由于线粒体蛋白平衡机制的改变在许多人类疾病中是常见的,包括癌症和神经退行性疾病,如阿尔茨海默病和帕金森病,怀斯曼指出,调节线粒体蛋白平衡的新细胞机制的鉴定,如Tim17A降解,提示了潜在的新的治疗方法来减弱线粒体功能障碍在这些疾病中。