基因测序项目发现儿童脑瘤的共同驱动因素
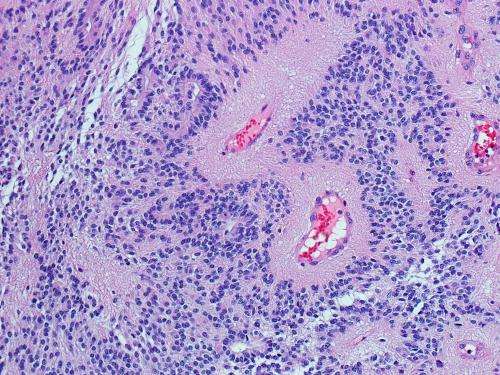
圣裘德儿童研究医院-华盛顿大学儿童癌症基因组计划已经确定了脑瘤室管膜瘤中最常见的基因改变,并有证据表明这种改变推动了肿瘤的发展。这项研究发表在2月19日的科学杂志上自然.
该结果为改进室管膜瘤诊断和治疗的新研究提供了基础,室管膜瘤是儿童第三大常见脑肿瘤。圣裘德已经开始致力于将这一发现转化为治疗这种疾病的新疗法,40%的年轻患者仍无法治愈这种疾病。这些发现也有助于理解和干预其他癌症,包括成人肿瘤。
新发现的变异涉及一种名为RELA的基因。该基因在NF-kappa-B通路中起着关键作用,NF-kappa-B通路是细胞中调节炎症的信号系统。研究人员早就认识到,这种途径在许多成人肿瘤中被不恰当地开启。这项研究标志着科学家们第一次在脑癌通路的中心部分发现了一个重复的错误——基因改变。
在这项研究中,70%患有大脑前部室管膜瘤的年轻患者携带了RELA改变和很少的其他遗传变化。在大脑其他区域的室管膜瘤中没有发现这种变化。
“在这项研究中,我们首次证明了NF-kappa-B通路中心的频繁突变足以将正常脑细胞转化为癌细胞并推动肿瘤的发展,”圣裘德综合癌症中心主任、医学博士、博士、联合通讯作者Richard Gilbertson说。“这应该有助于我们了解异常的NF-kappa-B活动是如何导致癌症的,并开发新的治疗方法来阻止这种活动。”
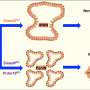
这种基因突变将RELA与另一个基因C11orf95的部分基因融合在一起,这一过程被称为易位。这种易位产生的异常蛋白质会迅速在小鼠体内引起致命的脑瘤。这些肿瘤与人类疾病相似。
“这是一个令人兴奋的发现,不仅对了解罕见的、特别具有毁灭性的儿童脑癌的生物学,而且对了解如何有效地治疗它,”圣路易斯华盛顿大学医学院基因组研究所所长、合著者理查德·k·威尔逊博士说。
圣裘德目前正在领导一项国际研究,以确定C11orf95-RELA易位是否有助于预测室管膜瘤患者的预后。圣犹达还开发了一种检测方法来识别携带易位的肿瘤。共同通讯作者David Ellison,医学博士,圣犹达病理学系主任,领导了这项工作。
圣犹大研究人员开发的一种名为CICERO的分析工具在识别易位方面发挥了关键作用。共同通讯作者Jinghui Zhang博士,St. Jude计算生物系的准成员,领导了开发CICERO的团队。
要找到这种易位,需要筛选2460亿条遗传信息,这些信息包含肿瘤的完整遗传密码,以及41名年轻室管膜瘤患者的正常DNA。研究人员还研究了77个室管膜瘤的RNA。细胞中的DNA包含每个基因的密码,而RNA将这些信息传递到细胞中制造蛋白质的部分。通过对DNA和RNA进行测序,科学家们可以看到哪些基因被激活并产生了异常产物,如RELA易位。
利用CICERO,研究人员发现RNA异常,导致他们发现C11orf95-RELA易位。融合基因是在容纳C11orf95和RELA基因的11号染色体片段被打碎并错误地重新组装时产生的。
其结果是脑肿瘤中最常见的易位之一。在这项研究中,41例开始于大脑前部的室管膜瘤中,29例肿瘤有易位制造出RELA融合蛋白。Gilbertson说:“改变导致异常蛋白质的事实提供了一个潜在的新的治疗靶点,这对室管膜瘤很重要。”
研究人员正在努力了解融合蛋白是如何导致癌症的。有证据表明,C11orf95通过改变RELA在细胞内移动并执行其正常功能的方式发挥着关键作用。研究人员还发现了可能导致室管膜瘤的其他基因易位。
这项研究是儿童癌症基因组计划的一部分,该计划已经对700名年轻癌症患者的正常和肿瘤基因组进行了完整的测序。该项目于2010年启动,旨在利用基因组测序技术的进步,提高对一些最具侵略性和最不为人知的儿童癌症的理解和治疗。
更多信息:C11orf95-RELA融合驱动室管膜瘤致癌nf - κ b信号通路DOI: 10.1038 / nature13109