科学家在该法案中捕获误导的DNA修复蛋白
Scripps研究所(Tsri)在加利福尼亚州的Scripts研究所(Tsri)领导的科学家们发现了一些涉及一种类型的DNA修复的关键蛋白质。
DNA损伤的积累会导致癌症的侵略性形式和加速老化,因此身体的DNA修复机制通常是健康的关键。然而,在一些疾病中,DNA修复机械可以变得有害。Scripps研究所(Tsri)在加利福尼亚州的Scripts研究所(Tsri)领导的科学家们发现了一些涉及一种类型的DNA修复的关键蛋白质。
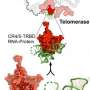
新研究的重点,发表于2014年5月22日版的期刊细胞报告,是一种称为Ring1b的蛋白质。TSRI研究人员发现Ring1B促进了融合端粒- DNA的序列,其在染色体末端充当保险杠并保护重要的遗传信息。科学家们还表现出抑制这种蛋白质可以显着降低受此类端粒功能障碍影响的细胞的负担。
“我们非常远离治疗,但我认为我们所识别的很多因素可以在加工功能失调端粒中发挥关键作用,肿瘤发生[癌症启动]的关键事件,”Tsri曾担任顾问领导了这项研究。
端粒的麻烦
人类诞生于长端粒,但每次在身体划分的细胞时都变短。随着年龄的增长,端粒变得非常短,特别是在具有高增殖率的组织中。
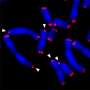
这是问题的开始。当端粒变得太短时,它们会失去端粒保护帽,并被DNA修复机械蛋白识别。这可能导致染色体“端到端”融合成串状形成。
连接的染色体代表一种异常的基因组排列,在分裂的细胞中是极其不稳定的。在细胞分裂时,连接的染色体可以破裂,产生新的断点,进一步重新参与异常DNA修复。这些融合和断裂的循环导致了猖獗的突变水平,这是癌症的肥沃土壤。
“你基本上争论了基因组,然后你有很多机会选择非常讨厌的突变,”拉泽桑尼迪尼克说。
设置DNA陷阱
要了解如何防止这些有害的融合,Lazzerini Denchi和他的同事希望确定所涉及的所有修复因素。
研究人员决定设定一个陷阱。使用基因工程细胞,研究人员能够除去称为TRF2的端粒结合蛋白。没有TRF2,端粒是未受保护的,并且募集DNA修复蛋白染色体末端,在那里它们促进染色体融合。
然后,研究人员被困并分离了他们发现与端粒结合的所有蛋白质。“这就像一个钓鱼探险,在我们的案例中的诱饵是端粒体DNA序列,”Lazzerini Denchi说。
克里斯蒂纳巴特科,在Lazzerini Denchi的实验室的博士后研究员,以及新的研究的第一个作者,花了两年多的时间,完善一种鉴定植物植物的蛋白质。“这是一个非常具有挑战性的实验,”她说。
然后,研究人员将蛋白质与DNA序列分开,并将蛋白质送到Tsri教授John Yates的质谱分析实验室。该分析显示了24种已知的修复蛋白和100种另外的蛋白质,其在功能障碍端粒中的作用尚未描述。
然后,团队改善了他们的搜索并仔细看看修复因素的作用蛋白质称为ring1b。这是第一次,科学家能够将Ring1B链接到染色体融合过程。Bartocci表示,Ring1b在功能失调的端粒修复中的作用是“非常引人注目”。
“如果你没有Ring1b,融合染色体的过程不是很有效,”Lazzerini Denchi说。
除了Ring1B之外,该团队还发现了近100个因素可能与DNA损伤修复中的误差有关。本研究的下一步是进一步细化DNA修复因子的长期列表,并研究可能影响人类健康的其他蛋白质。
进一步探索











用户评论