研究将衰老与线粒体的氧化损伤联系起来
只要人类还活着,他们就一直在寻找延长寿命的方法。到目前为止,还没有人发现青春之泉,但研究人员已经开始逐渐了解人类是如何衰老的,这为减轻时间对身体影响的疗法带来了希望。
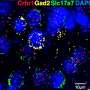
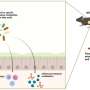
在一项新的研究中,宾夕法尼亚大学的科学家们利用创新技术找到了线粒体(细胞中将食物转化为能量的小隔间)氧化损伤可能在衰老过程中发挥作用的证据。
宾夕法尼亚大学兽医学院动物生物学系助理教授布雷特·考夫曼(Brett Kaufman)是这项研究的资深作者,该研究发表在该杂志上自由基生物学与医学“,.考夫曼实验室的博士后研究员吉尔·科勒萨(Jill Kolesar)是这项研究的第一作者。考夫曼和科勒萨与加拿大麦克马斯特大学的一个团队合作,该团队包括阿德尔·萨夫达尔、阿坎·阿巴迪、劳伦·麦克尼尔、贾斯汀·克兰和马克·塔诺波尔斯基。
线粒体被称为细胞的“发电站”。它们将我们所吃的转化为我们用来生长、运动和生活的能量。但是线粒体还有一个特殊的特征:它们包含自己的基因组,而且是多份拷贝。与遗传自双亲的核基因组不同的是线粒体基因组只能通过母系遗传。
尽管线粒体DNA与核DNA相比很小——16000个碱基对,而不是30亿个碱基对——但它至关重要。
考夫曼说:“在进化的过程中,它被减少了很多,以至于很少有核苷酸可以变化。”“当出现序列变异、线粒体DNA缺失或缺失时,疾病和病理就会发生。”
事实上,研究表明线粒体功能障碍在心脏病、癌症、肌肉萎缩症和阿尔茨海默病等多种疾病中起着主导或辅助作用。它也与衰老有关。
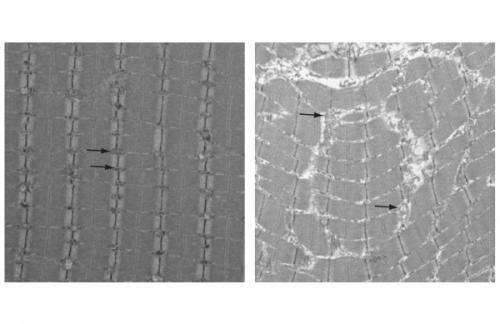
在这项新研究中,考夫曼和他的同事们检查了一只突变老鼠,这种老鼠被培育成线粒体功能失调的老鼠,结果过早地显示出人类衰老的特征。在一岁的时候,这对老鼠来说是中年早期,这些动物有灰色的头发,肌肉量减少和心脏病。
其他研究人员也研究了同一种小鼠,但没有发现证据氧化应激这种情况发生在线粒体产生更多的时候活性氧即ROS,是细胞在损伤发生前可以清除的物质。宾夕法尼亚大学领导的研究小组假设,氧化应激可能是这些小鼠过早衰老的部分原因。
考夫曼说:“你呼吸的90%的氧气被线粒体用来制造能量。”“有时电子在这个过程中会出错,可能会击中它们不应该遇到的东西,比如离得很近的线粒体DNA。理论是,随着我们年龄的增长,我们会产生更多的ROS,对线粒体造成更多的损害,这就形成了一个恶性循环。”
研究人员使用考夫曼实验室开发的复杂技术来仔细研究突变小鼠的线粒体DNA。他们发现了损伤的证据,包括缺失、损耗和复制问题。对肌肉细胞施加额外的氧化应激以剂量依赖的方式导致类似的结果。
虽然其他研究人员没有发现氧化应激的标志,但考夫曼和同事们只检查了突变小鼠肌肉细胞中的线粒体,与正常小鼠相比,他们确实发现了与氧化相关的蛋白质水平增加。此外,他们还发现突变小鼠主要抗氧化剂的水平降低了,抗氧化剂是帮助清除组织中的活性氧的分子。
考夫曼说:“我们展示了第一个真正可靠的证据,在这个小鼠模型中,实际上存在线粒体氧化应激。”“当我们观察与解毒相关的分子途径时,我们发现这些小鼠的活动水平较低。这也是我们在衰老和久坐的生活方式中看到的。”
虽然研究小组没有在这只老鼠身上发现的氧化应激和缺陷之间建立直接联系,但他们的发现表明,氧化应激很可能在衰老过程中发挥作用。因此,保存线粒体DNA的含量和完整性可能是对抗与年龄有关的健康下降的一种策略。
“我们通常可以用抗氧化剂来做到这一点,更具体地说,可以使用靶向氧化的化合物线粒体考夫曼说。
该团队的下一步将是使用他们的新技术来检查涉及线粒体缺陷的其他疾病模型,包括心脏病早产和糖尿病。
进一步探索