用于罕见的阵发性夜间血红蛋白尿的药物获得FDA孤儿身份
近日,美国食品药品监督管理局(FDA)批准了一种由宾大制药公司研发的药物,用于治疗突发性夜间血红蛋白尿(PNH),这是一种罕见的、危及生命的疾病,由于红细胞破坏和血栓形成而导致贫血。这是在欧洲药品管理局(EMA)批准该药物的相同状态后不到两个月的时间。
这种名为AMY-101的药物被命名为孤儿药,这将使目前正在开发该化合物的Amyndas公司得以加快临床开发。Amyndas计划于2015年将AMY-101移入临床进行首次人体试验。AMY-101是一种对抗PNH的新方法,目前只能用美国出售的最昂贵的药物治疗。新的策略是基于抑制C3——人类免疫系统最古老部分的核心组成部分——被称为“补体”——对这种罕见的血液疾病的大多数患者来说,结果可能是更便宜和更有效的。
如果药物被FDA批准,这种特殊的孤儿状态允许七年的市场推出七年,并使孤儿药物制造商能够申请研究资金,税收抵免的某些研究费用,并帮助临床研究研究设计。该状态还提供了来自FDA的处方药用户费的豁免,该用户费用授权FDA从毒品提案国收取收费,以扩大其员工,以便更快地审查新药。
John Lambris,博士,博士博士,佩尔曼医学院病理学和实验室医学系的研究医学系,在宾夕法尼亚州发达了Amy-101,大学在Amyndas授权它,这是现在进一步开发化合物以在诊所施用。
“接受孤儿药品FDA和EMA的名称是AMY-101的发展途径中的重要成就和一个关键的里程碑,我们对这种有效补体抑制剂的长期潜力持乐观态度,“莱布布里斯说。”Amy-101可以代表对目前可用于PNH的治疗的显着治疗优势。“
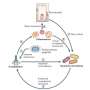
PNH影响每百万人中有1 - 5人,是由血细胞表面调节蛋白表达缺陷引起的,使血细胞容易受到补体攻击。这可能导致红色过早死亡血细胞这一过程被称为溶血,会导致严重的贫血,并有很高的凝血风险。AMY-101驯服这种不适当的补体激活,保护细胞表面免受攻击。
尽管存在一种治疗PNH的方法,三分之一的患者仍然需要输血来控制他们的贫血。这种无反应是由于补体C3蛋白片段在其表面的积累红细胞,最终会被免疫细胞攻击。研究小组利用人类PNH细胞研究了AMY-101对自我攻击和由此产生的溶血的影响,发现它是活跃的。











用户评论