遗传标记可以帮助预测肾移植的成功
肾脏捐赠的出生的人与一个小代码的一个关键基因的变化可能是更有可能的是,一旦移植接受者中,积累疤痕组织,导致肾功能衰竭,领导的一项研究显示伊坎在西奈山医学院的研究人员和今天发表在临床研究杂志。
如果进一步的研究证明变化导致纤维化(疤痕)的肾脏移植受者,研究人员可以用它来更好的屏幕潜在的捐赠者,提高移植的结果。此外,揭示蛋白质途径触发肾脏纤维化可能帮助研究人员设计的药物预防这种疾病过程中肾移植受者,也许在所有慢性病患者肾脏疾病。
“这是至关重要的,我们确定新的治疗目标,防止疤痕移植肾脏内,和我们的研究相关的遗传标记,和相关蛋白通路,糟糕的结果肾移植芭芭拉·墨菲说:“医学博士,椅子,医学系,默里·m·罗森博格的医学教授(肾脏学)和临床集成和人口健康主任伊坎在西奈山医学院。“药物设计者也许很快就能目标这些机制。”
常用的研究类型,全基因组关联研究(GWAS)看起来差异在许多点的遗传密码,看看,在人口,任何给定的变异在遗传密码是经常发现在那些与给定特征;在目前的研究中,增加了接受捐赠的肾脏的纤维化。
即使是最小的基因变异,称为单核苷酸多态性(snp),可以产生重大影响的特征通过交换一个32亿“字母”的人类DNA代码。当前研究发现统计上显著的关联基因的SNP确认为rs17319721 SHROOM3和进步肾瘢痕(纤维化)和一组功能损失肾脏捐赠者,主要是欧洲血统的。在许多情况下,某些单核苷酸多态性在家庭或民族将更加普遍。
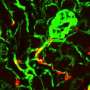
肾脏过滤血液清除多余的血糖和废物产品渗透肾管尿液,而re-absorbing关键营养物质。的累积疤痕组织在这些微妙的结构随着时间的推移将干扰正常的肾功能。
慢性肾脏疾病已经影响了10%的美国成年人和其患病率增加。随着导致肾功能衰竭在许多情况下,慢性肾脏疾病会增加心血管疾病的风险。纤维化肾小管是一种常见的致病过程中对于许多类型的慢性肾脏疾病和慢性疾病的核心部分捐赠肾脏(慢性移植物肾病,或者可以)。
可以有一个稳定,捐赠的肾脏功能逐渐丧失。相当比例的慢性肾脏疾病患者和纤维化肾小管最终将发展为肾功能衰竭,需要透析或移植肾脏的,更高的供应与需求。到目前为止,还没有有效的治疗预防肾脏疾病的进展。
研究者和临床医生作出了巨大收益在预防移植排斥在前几年通过选择性地抑制免疫系统,但长期损害和疾病仍然是一个重大的挑战。最终发展的分析来预测是否捐赠的肾脏移植后,会更容易受到炎症或疤痕可能有助于克服这一挑战。
新途径揭示药物靶点
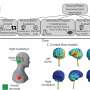
的临床研究杂志研究发现,基因的SNP rs17319721 SHROOM3,当出现在肾脏的捐赠者,与SHROOM3基因的表达增加,和一个更大数量的SHROOM3蛋白质在器官移植。SHROOM3打开更多的转录因子2 (TCF7L2) 7。反过来,这取决于几个基因与许多功能细胞。TCF7L2属于Wnt信号通路,并最终导致增加信号通过转化生长因子β1 (TGF-β1)和增加COL1A1表达式。
建设TGF-β1信号结缔组织(疤痕),通常恢复组织架构作为治疗的一部分,但也可能推动纤维化在错误的上下文。COL1A1 (I型胶原蛋白,α1)的编码基因I型胶原蛋白的主要成分,结缔组织的主要蛋白质成分(如骨。软骨)和伤口愈合的疤痕组织形式。在一起,这些因素导致多余的组织纤维化。
虽然SHROOM3被早些时候与慢性肾脏疾病相关工作,具体的作用和机制SHROOM3导致移植损伤和肾纤维化是未知的进入本研究。
当前的研究结果从一个正在进行的nih资助的专门研究肾移植受者(基因组学慢性同种异体移植物排斥反应(GOCAR)研究]。研究小组进行活检的移植肾脏移植后在预先确定的时间点和匹配的基因激活(表达式)水平在移植的肾脏移植后3个月的移植功能障碍指数12个月。
SHROOM3基因之间的联系,相关蛋白通路和纤维化检测全基因组关联研究中被证实在小鼠的人类肾脏疾病的模型。
“进一步的工作是要研究的临床应用之前,”墨菲博士说。“然而,我们的研究结果是一个至关重要的和乐观的一步改善治疗慢性肾脏疾病。"