研究人员发现食欲控制涉及的新型信号通路

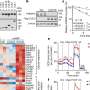
一项新的研究揭示了大脑中分子信号系统的重要细节,该细节与体重和代谢的控制有关。该研究于1月19日发表自然,提供对黑素皮质素途径的新理解,并可能导致肥胖症的新疗法。
加州大学圣克鲁斯分校的化学和生物化学杰出教授Glenn Millhauser合着者说,这些发现非常令人兴奋,并且具有广泛的生物医学含义。米尔豪瑟说:“我们正在进入控制大脑中这种重要的信号系统的真正分子特征。”
这项研究由范德比尔特大学的研究人员领导,重点是嵌入在称为黑色素素4受体或MC4R的神经细胞膜中的受体。它属于一类称为g-的受体蛋白质罗杰·康恩(Roger Cone)表示,耦合受体(GPCR)通常像开关开关一样,在短时间内发出信号。
Cone说:“这一发现确定了一种分子机制,用于将开关转换为变阻器。”“这可能有助于解释缓慢,持续的生物学过程,这些过程也由GPCR介导,例如晒黑或节食后恢复体重。”
Millhauser的实验室对与MC4R受体结合的蛋白质进行了广泛的研究,例如与Agouti相关蛋白(AGRP)。AGRP是一种有效的食欲刺激剂。Millhauser说,它在调节能量平衡方面的作用是抑制新陈代谢并增加喂养时,当人体需要减轻体重和储存能量时。他的实验室开发了改变其活性的AGRP蛋白的改良版本。在新的研究中,Millhauser实验室的修饰蛋白质帮助研究人员确定了先前未经引起的AGRP效应。
Millhauser先前的研究表明,给实验动物的一剂AGRP可以刺激每日食物摄入量长达10天。该观察结果与它与MC4R结合的受体的传统“关闭”信号模型不符。G蛋白耦合受体在关闭之前只能采取如此多的刺激,而这种称为脱敏的现象通常会迅速发生。
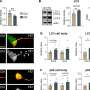
Cone的实验室发现了一种伴随蛋白,这是一种称为KIR7.1的钾通道 - 与MC4R受体偶联,并独立于G蛋白信号传导起作用。研究人员发现,AGRP诱导MC4R打开钾通道,该钾通道“超极化”并抑制涉及阻断食欲的神经元。
Millhauser说:“此外,随着对我们实验室先前发现的AGRP的修改,我们可以增加或减少受体与钾通道的耦合。”“这些概念最终可能导致新一代的治疗代谢性疾病的治疗剂,包括肥胖,厌食症和卡希克西氏症,这通常在癌症治疗中发生。”
进一步探索