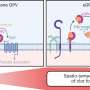
用于关节修复的无支架iPS细胞透明软骨
膝关节疼痛和其他关节疼痛在老年人中是正常的,有时甚至在年轻人中也是如此。虽然这些疼痛很少会危及生命,但患有这些疼痛的人知道这对生活质量造成的负担和影响。在许多情况下,原因是透明软骨的丧失,它没有再生的能力,这意味着一旦失去它就永远消失了。它们不包括I型胶原蛋白,这是纤维软骨或疤痕组织中的主要胶原蛋白。成功恢复的关键是将只分泌透明软骨ECM蛋白的软骨细胞引入退化的软骨。
自体软骨细胞移植是治疗透明软骨损伤最常用的方法之一。这项技术包括从活检组织中获得透明软骨,然后将其移植到受伤部位。因为活检组织比需要修复的区域要小,所以软骨细胞必须扩大,这一任务需要对ECM蛋白进行酶解。不幸的是,扩张导致软骨细胞分泌I型胶原蛋白,这就是为什么在这种手术后,纤维组织的存在是不可避免的。因此,“软骨细胞失去了它们的软骨属性”,京都大学iPS细胞研究与应用中心的Noriyuki Tsumaki教授说。
为了解决这个问题,Tsumaki和他的团队与KU医学院的Shuichi Matsuda教授领导的小组合作,报告了一种新的方案,该方案不扩展软骨细胞,而是扩展iPS细胞。当扩增出足够数量的iPS细胞时,该方案要求研究人员将这些细胞分化为软骨细胞。因为这些软骨细胞是直接从iPS细胞中分化出来的,所以不需要消化ECM蛋白,这就避免了纤维组织并且只能合成透明软骨。
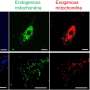
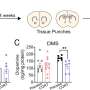
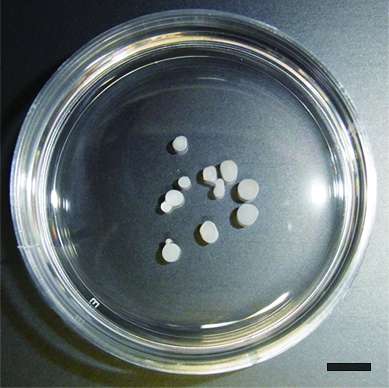
这种方法的另一个优点是避免使用人工支架。在其他关于ES细胞和ipsc来源的软骨细胞移植的研究中,人工支架被包括到移植中,以提供支持,直到软骨细胞开始分泌自己的ECM蛋白。然而,目前尚不清楚人工材料是否会阻碍软骨的最佳整合。因为软骨细胞已经开始分泌ECM蛋白,它们可以在没有支架的情况下被移植。这一特征归因于使用含有BMP2、TGFβ1和GDF5的悬浮培养和培养基6周。在此之后,软骨细胞停止增殖并开始分泌透明质软骨纯度高的ECM蛋白。这种软骨细胞和ECM基质蛋白的混合物被收获为直径1-2毫米的颗粒,可以直接移植到损伤组织中(图1和2)。每个颗粒含有大约7万个软骨细胞,根据Tsumaki的说法,这是一个很好的理由相信足够的细胞用于人体移植是可行的。“一百万软骨细胞需要处理1平方厘米的缺陷,典型缺陷的面积为2-10平方厘米。因此,我们正在考虑移植30-150个颗粒。这些数字是相当可控的。”
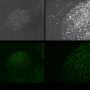
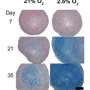
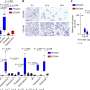
研究小组将他们的颗粒移植到三种动物模型中:小鼠、大鼠和迷你猪,发现了整合和维持的积极迹象(图3)。这些结果只鼓励了Tsumaki。“这些发现只是初步的,但它们显示出良好的安全迹象。下一步是在我们考虑患者治疗之前,在更大的动物身上找到移植的最佳条件。”
-
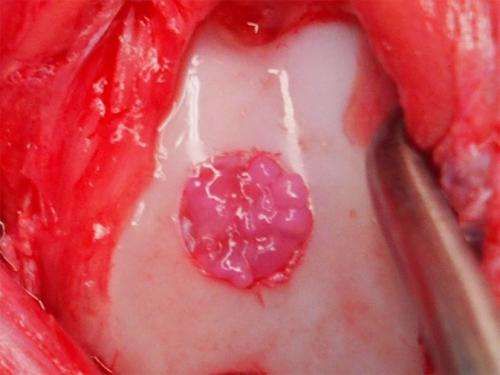
图1中的颗粒可以在白色软骨内的粉红色圆圈中看到。图片来源:Tsumaki Noriyuki教授干细胞报告 -
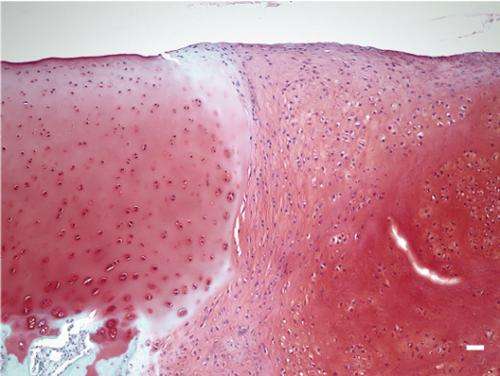
此图显示股骨内原生软骨(深紫色)和移植软骨(浅紫色)。黑点为软骨细胞核。图片来源:Tsumaki Noriyuki教授干细胞研究