研究人员描述新方法,促进心脏组织的再生
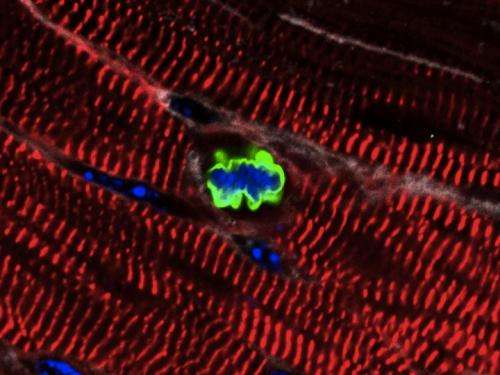
哺乳动物的心脏组织受伤后再生能力有限,如心脏病发作,部分原因在于无法激活心肌细胞增殖程序。最近的研究表明低水平的心肌细胞(心肌细胞)增殖在成年哺乳动物,但这不足以修复受损心脏。
领导的研究小组Ed Morrisey博士,医学教授和细胞和发育生物学和再生医学科学研究所主任在宾夕法尼亚大学佩雷尔曼医学院,现在已经表明,RNA分子的一个子集,称为小分子核糖核酸,对心肌细胞是重要的细胞增殖在开发和足以导致心肌细胞增殖在成年人的心。不生成的小分子核糖核酸,蛋白质,通过信使rna结合,抑制基因表达,蛋白质生成,并促进其降解。这个发现出现在本周科学转化医学。
研究小组发现微群的损失mir302 - 367小鼠导致减少在开发过程中心肌细胞细胞增殖。相比之下,微rna的表达增加集群在成人心脏通常是非成人心肌细胞活化增殖。
这发生了复活,在某种程度上,通过镇压被称为“河马”的手段,控制细胞增殖和器官大小。“河马通路通常压制时细胞增殖。集群mir302 - 367目标河马通路中的三个主要的激酶组件,减少途径活性,心肌细胞可以重新进入细胞周期并开始再生心肌,”Morrisey解释道。“这是一个压抑的情况下抑制因子”。
在成年小鼠,表达的微群重新激活心肌细胞的细胞周期,导致减少疤痕形成一个实验性心肌梗死损伤后诱导的小鼠。也有增加心肌细胞的数量相同的老鼠。
然而,长期的表现超过几个月的microRNA集群造成心肌细胞de-differentiation和变得不那么实用。“这建议我们,持续活化的细胞周期在成人心肌细胞可能是有害的,导致心脏失败,“Morrisey说。研究人员猜测,心肌细胞可能需要de-differentiate分裂,但他们可能会失去他们合同的能力。
“我们克服这个限制,注入合成小分子核糖核酸和一个叫模仿的短半衰期的老鼠,”Morrisey说。模拟治疗心肌梗塞后七天导致心肌细胞增殖和再生所需增加的新心肌,导致减少受伤后纤维化和改善心脏功能。
重要的是,研究小组发现,短暂的七天的治疗并没有导致心脏功能的逐步丧失,增加微rna表达的遗传模型。整体而言,这些结果表明,任何治疗,改善心脏再生促进心肌细胞增殖的可能需要暂时避免的有害影响,保持高水平的扩散并在组织,通常non-proliferative de-differentiation。
“这项研究的下一阶段是确定microrna的模仿是否会工作在一个更大的动物模型和与工程师们合作创建一个本地交付系统的心脏,而不是让系统,“Morrisey指出。
进一步探索








用户评论