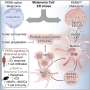
研究确定了致命的前列腺癌的亚型
科罗拉多大学癌症中心的一项研究发表在杂志上癌症研究“致命”的定义了一个新的、不同的亚型前列腺癌,两个基因的损失,MAP3K7 CHD1。整体约10%的前列腺癌患者将死于该病。前列腺癌患者的研究表明,组合MAP3K7 CHD1删除,约50%前列腺癌复发,最终导致死亡。大约10%的前列腺癌港结合MAP3K7-CHD1删除。
“这是一个多学科的研究由多个调查人员在多个机构是一种极具威胁性的前列腺癌癌症能杀死人,”斯科特•克莱默博士说,研究员铜癌症中心、铜医学院药理学系教授,和文章的资深作者。
克莱默和铜的同事包括林赛•罗德里格斯博士,博士詹姆斯•科斯特洛和斯科特·露西亚,医学博士,从很早以前开始观察到一些前列腺癌往往是缓慢和不那么危险,而别人往往是快速增长的和危险的。问题是是否有攻击性,而且不那么咄咄逼人前列腺癌基因的区别。分析肿瘤样本公开数据库显示,MAP3K7-CHD1损失是癌症的主要遗传标记的最终成为积极的类型,可能是前列腺癌症相关死亡的占25%。每年约有7500人。克莱默实验室然后使用一个复杂的人工前列腺肿瘤干细胞模型发展与这些基因植入老鼠的删除。
“这是一个独特的模式,”克莱默说。“我们种植小鼠前列腺干细胞细胞在文化中,我们撞倒了这两个基因。然后我们把这些工程干细胞与前列腺癌的细胞使人工前列腺和移植到我们的小鼠模型。这允许我们前瞻性观察前列腺生长的看到这些特定的基因变化的影响。”
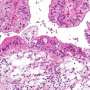
事实上,这些人工前列腺腺体生长在老鼠发达侵略性癌症类似的人类癌症的数据库。具体来说,损失的基因MAP3K7 CHD1”极大地扰乱了“前列腺癌干细胞的能力来创建健康的前列腺组织,而相反,他们创造了癌细胞“神经内分泌和神经细胞的特征。换句话说,这个基因变化使干细胞应该创建健康的前列腺组织,而不是创建混合型细胞破坏的许多控制管理复制和增长速度。正是这些混合细胞癌大举行动。
“现在的目标是发现这些致命的目标的方法前列腺癌细胞,”克莱默说。第一个包含一个“合成致命的“屏幕测试成千上万的候选药物对细胞MAP3K7-CDH1删除识别药物选择性地与这些删除杀死细胞。克莱默和他的同事们还计划额外的测试,进一步完善这些删除的预后能力的测试。
“这可能使之间的差异选择等等看前列腺癌,对治疗更积极,”克莱默说。在这项研究中使用的干细胞模型重要的未来的研究可能会提供一个平台。
进一步探索