新的见解可能会导致对抗阿尔茨海默氏症的治疗策略的改变
阿尔茨海默患者患者的大脑的典型特征是存在不溶性的Tau蛋白聚集体。VIB,Ku Leuven and Janssen Pharmaceutica的科学家已经证明,通过脑细胞之间的突触连接促进了通过大脑的这些聚集体的分布。这个消息非常重要,因为重点越来越多地用于修复突触连接作为诸如Alzheimer等神经变性疾病的治疗策略。事实上,普遍认为,突触连接的损失导致认知技能的损失。
Dieder Mochars(Janssen Pharmaceutica):“看着我们的结果,我们会建议谨慎关于修复突触的治疗方法。我们的研究表明突触还促进了Tau骨料的分布,这可能抵消修复突触的积极影响。在开发新的治疗策略时,例如通过将突触恢复方法与将在突触中删除Tau骨料的突触恢复方法相结合,这也很重要。“
Patrik Verstreken (VIB/KU Leuven):“我们已经专门为这项研究建立了一个新的体外系统,使我们能够研究聚集蛋白在整个大脑中的分布,这是神经退行性疾病的典型特征。我们还想利用这个系统来探索哪些物质可以在不使用早期动物模型的情况下抵消大脑神经退行性变的进展。这可能会成为寻找治疗阿尔茨海默氏症(Alzheimer's disease)等潜在药物的重要工具。”
突触
脑细胞通过突触进行通信。成功的突触连接是至关重要的,以便正常运作。突触变性是一种症状神经退行性疾病如阿尔茨海默氏症。阿尔茨海默氏症中,突触的丧失会导致认知能力。这就是为什么正在进行大量研究的治疗,其关注于修复突触。
与VIB,Ku Leuven和Janssen Pharmaceutica,Sara Calafate,Patrik Verstreken和Dieder Mochars一起一起发现这种方法并不简单。
Sara Calafate:“我们注意到Tau骨料的传播,Alzheimer的典型特征,通过互连更有效地进行了更有效大脑细胞。但目前还不清楚突触在这一过程中扮演了什么角色。我们现在已经成功地证明了这一点突触促进这种分布,可能会促进神经变性。”
一种新的体外模型
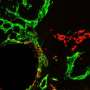
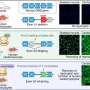
科学家为这项研究开发了一种新的研究工具,使他们能够监测Tau蛋白聚集物的扩散,同时改变脑细胞之间的突触连接。他们在显微镜下的小房间里培养脑细胞,使突触连接与其他细胞分离成为可能。当突触连接形成时,研究人员观察到Tau蛋白的分布比没有突触连接时的效率高50%。
patrick Verstreken:“没有动物模型,我们对大脑疾病的研究是不可能的。然而,我们一直在寻找减少动物实验数量的方法。这个新工具可以帮助我们实现这一点。”
进一步探索
www.ncbi.nlm.nih.gov pubmed / 25981034










用户评论