肌营养侧向硬化和额光痴呆基因的新小鼠模型
佛罗里达州梅奥诊所的研究人员开发了一种小鼠模型,表现出与最常见的肌营养的外壳硬化(ALS或Lou Gehrig疾病)和额定颞痴呆症(FTD)相关的神经病理和行为特征,这是由突变引起的C9ORF72基因。
他们说他们的发现,今天报道了科学,将进一步研究这些疾病背后的分子机制,而且动物模型将提供一种方法来测试潜在的治疗剂,以阻止大脑和脊髓中神经元的死亡。
“我们的小鼠模型表现出ALS和FTD的病理和症状在患者中C9ORF72.突变,“研究的高级作者,Leonard Petrucelli,Ph.D.,Ralph B.和Ruth K..Belams和佛罗里达州梅奥诊所神经科学系的教授和主席。
根据ALS协会的说法,超过30,000名美国人住在于ALS,一种破坏电机神经元细胞的病症,可控制必要的肌肉活动,如说话,行走,呼吸和吞咽。在阿尔茨海默病之后,圆颞痴呆症是最常见的形式早期发病痴呆。它的特征在于脑正面叶中神经元损失的人格,行为和语言的变化。根据阿尔茨海默氏症的协会,曾经被认为罕见的,FTD现在考虑到所有痴呆症案件的高达10%至15%。
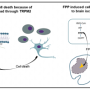
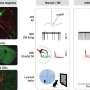
新的小鼠模型表明了C9ORF72.重复扩张,2011年通过Mayo Investigator Rosa Rademakers发现的遗传异常,Ph.D.,导致形成异常焦点或丛的有毒核糖核酸(RNA)物种,以及C9ran和TDP-43的夹杂物蛋白质。Petrucelli实验室发现了FTD和ALS病例中C9ran蛋白的存在C9ORF72.2013年的突变(C9FTD / ALS)。然而,新的研究揭示了灯光C9ORF72.重复膨胀和夹杂物的TDP-43,一直众所周知的蛋白质在大多数ALS和FTD病例中唤起了AWRY。在阿尔茨海默病患者和经历头部受伤或重复脑震荡的人中也发现了TDP-43夹杂物。
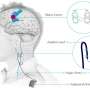
调查人员报告了这些小鼠大脑的物理和生化变化可能负责观察到的行为缺陷和类似于人类疾病症状的运动障碍。在六个月的年龄,表达扩张的小鼠C9ORF72.在整个中枢神经系统中重复表现出多动,焦虑,反社会行为和电机缺陷。
“在这些小鼠中找到TDP-43完全是意想不到的 - 我们无法在重复扩展之间发现链接C9ORF72.帕雷加利博士说,在没有鼠标模型的情况下的TDP-43病理学的发展。“
“这是一个非常令人兴奋的观察,”他说。“我们尚不知道焦点和C9RAN蛋白质与TDP-43异常相关或途径是如何,但随着我们的新动物模型,我们现在有办法找出答案。”
通过与佛罗里达州斯克希普研究所的合作,Petrucelli实验室还正致力于鉴定与重复膨胀RNA结合的化学化合物,然后才能形成破坏神经细胞功能的焦点和C9RAN蛋白质。通过治疗RNA治疗RNA,从而防止在脑细胞中形成RNA焦点和C9RAN蛋白质,合作者希望对抗C9FTD / ALS患者遭受的患者死亡和相关的疾病症状。不仅是新的鼠标模型对于测试新型化学化合物是有用的,小鼠的研究结果表明,一种减轻与焦点和C9RAN蛋白相关的毒性的药物也将预防TDP-43病理学。
进一步探索








用户评论