科学家认为干扰素β在持续的病毒感染中可能是罪魁祸首

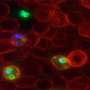
干扰素蛋白通常被认为是病毒战斗机,但是Scripps研究所(TSRI)的科学家发现了证据,表明其中一个,干扰素β(IFNβ)具有免疫抑制作用,可以帮助某些病毒建立持久感染。
结果表明,阻止IFNβ的药物可能有一天被用来治疗持续的病毒感染,其中包括HIV和丙型肝炎和C感染。
TSRI研究人员的高级研究员Michael B. A. Oldstone说:“我们发现,IFNβ对于在持续感染中看到的免疫抑制作用很重要,即使它通过IFNα蛋白使用的相同受体的信号,其作用非常不同。”出现在2015年5月13日发行细胞宿主和微生物。
制动还是煤气踏板?
大约60年前发现的干扰素是细胞对病毒侵袭的分泌的蛋白质之一。它们已知的功能包括激活T细胞,干扰病毒复制并增强病毒蛋白向免疫系统的呈现。长期以来,它们一直被认为是抗病毒和促进免疫,实验室成长的I型I型蛋白用于治疗丙型肝炎感染和一些癌症。
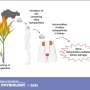
然而,很明显,干扰素不仅会促进免疫系统。在报道的一项研究中科学例如,在2013年,Oldstone和他的实验室发现了I型干扰素信号传导对免疫反应具有强大的制动作用的证据,这种制动效应可能通过感染病毒以增强其生存而进行的制动效应。Oldstone Notes阻断了I型干扰素受体信号传导校正了病毒诱导的次级淋巴组织的混乱,使T细胞在淋巴样组织中的T细胞迁移,并减少负责流产病毒特异性T细胞活性的分子控制病毒感染。
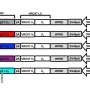
对于新研究,Oldstone和他的团队试图确定IFNα或IFNβ是否负责该制动效应。IFNβ是主要嫌疑人。在鼠标模型中持续感染,它使用了鼠标感染的LCMV病毒的变体(“克隆13”),IFNβ在小鼠的水平上产生的水平要高得多,而非持久性LCMV变体(ARM 53B)的水平要高得多。在包含LCMV CL-13或ARM的3,356个氨基酸中,这些病毒仅由三个氨基酸差异。其中之一是在LCMV GP-1尖峰中,负责与宿主细胞的受体和进入的结合,而第二个位于聚合酶蛋白中,与LCMV Cl 13 1.5至2 logs的复制相关,比LCMV在LCMV中的复制增强相关。树突状细胞。此外,据报道,IFNβ具有抗炎作用,并用于治疗自身免疫性疾病多发性硬化症,尽管其精确的作用机理尚不清楚。
选择系统
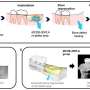
该小组,包括第一作者Cherie Ng,当时是一名Oldstone实验室的研究助理,检查了没有IFNβ和正常小鼠基因的小鼠,其中IFNβ活性被单克隆抗体阻塞。
该实验表明,没有IFNβ信号传导的LCMV CL-13感染的小鼠恢复了淋巴机结构,并增强了用于攻击LCMV的T细胞。到感染的第30天,与完整的IFNβ信号传导相比,小鼠在脾,肝脏,肺和血液中的病毒载量也明显降低。
相比之下,用中和六个亚型的抗体阻断IFNα没有这些有益作用。此外,阻断IFNα活性导致感染早期的病毒扩散。这些结果暗示,尽管IFNα和IFNβ通过相同的细胞受体信号,但IFNα蛋白在限制早期病毒扩散方面很重要,而IFNβ是一种免疫抑制分子。
“研究人员长期以来一直假设干扰素不仅为了冗余而进化了许多不同的亚型,而且因为这些亚型具有不同的生物学作用,”奥尔斯通说。“就IFNβ而言,该作用可能是遏制免疫反应,从而防止由于这种免疫反应而导致的过度损害和自身免疫性。”
奥尔斯通说:“ LCMV CL-13以及可能持续存在(可能是癌症)的其他病毒已经学会了选择免疫抑制功能以中止消除它们所需的T细胞功能。”
Oldstone及其团队的下一步包括精确确定IFNα和IFNβ蛋白与IFN-I受体的结合如何不同,这些结合如何改变免疫相关基因的表达以及IFNβ途径上的哪些点可以最好地用药物靶向治疗持续感染,也许还有一些癌症。