视力光明:向获得性失明的潜在疗法迈进了一步

遗传性失明是由眼睛中的感光细胞(即感光细胞)逐渐退化引起的,影响着全世界数百万人。尽管感光细胞消失了,但视网膜深层的细胞却完好无损,这些细胞通常无法感知光线。一种基于“光遗传学”技术的有前途的新治疗方法是将光敏蛋白质引入这些幸存的视网膜细胞,将它们变成“替代光感受器”,从而恢复视力。然而,一些因素限制了使用传统光敏蛋白进行临床光遗传治疗的可行性,因为它们需要不自然的高强度和潜在的有害光强度,并在目标视网膜细胞内使用外部信号机制。
新的研究发表在5月7日的《开放获取》杂志上公共科学图书馆生物学van Wyk和他的同事展示了如何定制光遗传蛋白,使这项有前途的技术更接近医疗应用。“我们在问这个问题,‘我们能否设计光激活蛋白,在特定细胞中打开特定信号通路?’换句话说,目标细胞的自然信号通路能被保留下来,并被修改成由光而不是由先前神经元释放的神经传递素打开的方式吗?”该论文的通讯作者Sonja Kleinlogel博士说(其研究小组位于瑞士伯尔尼大学)。分子工程的目的是实现与天然信号的最大兼容性,同时保留传统光遗传蛋白的所有优点,如快速动力学和抗光漂白。
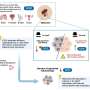
这种新型的光敏蛋白被称为optical - mglur6,是一种由视网膜光色素黑视素的光敏结构域和ON-bipolar细胞特异性组成的嵌合蛋白代谢性谷氨酸受体mGluR6,它被光感受器释放的谷氨酸自然激活,并通过耦合的细胞内酶途径放大传入信号。例如,与视紫红质不同,黑视素的“光天线”可以抵抗漂白。换句话说,optomglur6的反应强度从未减弱,无论蛋白质被光击中的频率和强度有多高。此外,由于optomglur6是一种由两种“局部”视网膜蛋白组成的嵌合蛋白,它也可能对免疫系统“不可见”,这是对传统光遗传蛋白的另一种改进。
在他们的研究中,van Wyk和同事们瞄准了视网膜上的双极细胞,这些细胞自然地接受来自视网膜的直接输入光感受器.以视觉级联顶端的存活细胞为目标具有最大限度地利用视网膜信号计算的优势。将天然化学受体(mGluR6)转化为光激活受体确保了on -双极细胞内天然信号的保存,赋予高光敏性和快速“正常”反应性。在他们的研究中,他们证明了患有色素性视网膜炎的老鼠可以通过治疗恢复日光视力。Kleinlogel博士说:“这种新疗法有可能使患有任何类型的感光器官退化的患者恢复视力,例如那些患有严重的老年性黄斑变性的患者,这是一种非常常见的疾病,在某种程度上,65岁以上的人中每10人中就有1人患有这种疾病。”
“新方法的主要改进是,患者将能够在正常日光条件下看到,而不需要光增强器或图像转换护目镜,”Kleinlogel博士进一步指出,“并且保留细胞内酶级联的完整性,因为酶级联在多个水平上被复杂地调制,mGluR6通过细胞内酶级联作用确保了视觉信号的一致性。”on -双极mGluR6受体细胞属于所谓的g蛋白偶联跨膜受体(GPCRs)大家庭。工程抗漂白嵌合光学- gpcrs的新原理打开了一个全新的可能性。例如,由于GPCRs是药物干预的主要靶点,Opto-GPCRs可能被用于治疗疼痛、抑郁和癫痫等疾病。
更多信息:van Wyk M, Pielecka-Fortuna J, Löwel S, Kleinlogel S(2015)在盲人视网膜中恢复ON开关:optical - mglur6,新一代细胞定制光遗传工具。公共科学图书馆杂志13 (5): e1002143。DOI: 10.1371 / journal.pbio.1002143