新的治疗希望肌营养的外侧硬化
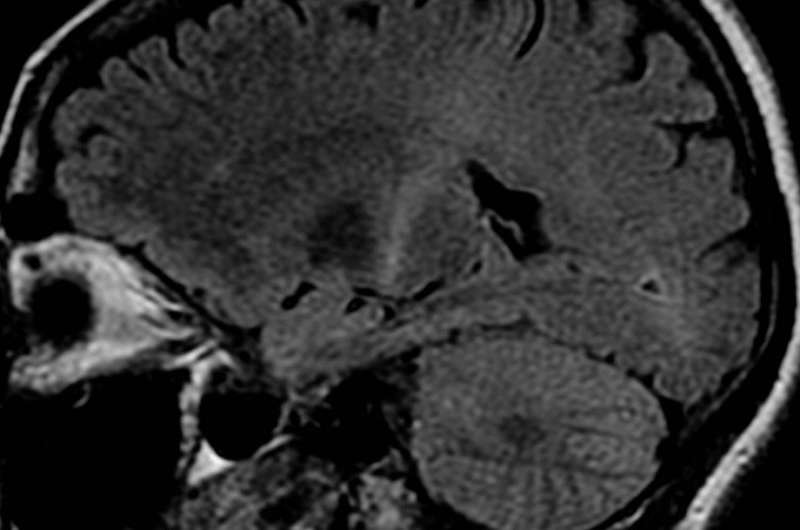
在Chum Research Center和蒙特利尔大学的科学家们发现了免疫系统和运动神经元在肌营养的外壳病变(ALS)中的肌肤神经元(ALS)之间的死亡,也被发现。该发现铺平了一种全新方法,用于寻找可以治愈或至少减缓这种神经退行性疾病的进展作为ALS,阿尔茨海默氏症,帕金森和亨廷顿疾病的药物。
今天发表的研究自然通信,表明了免疫系统在动物模型C.埃贝朗斯,一个小小的1毫米的蛔虫,在ALS的发展中起着关键作用。'免疫系统的不平衡可能有助于破坏运动神经元蒙特利尔大学神经科学系的亚历克斯帕克,Crchum研究员和副教授塞克斯帕克,Crchum研究员和副教授。
肌萎缩的外侧硬化是一种攻击神经元和脊髓的神经肌肉疾病。受影响的人逐渐变得瘫痪,通常在症状发作后少于五年。这种破坏性痛苦目前没有有效的补救措施。Riluzole,唯一批准的药物只会将患者的生命延长了几个月。
十几个基因与ALS有关。如果其中一个突变发生,则该人会出现这种疾病。科学家将突变的人类基因(TDP-43或FUS)引入C.秀丽隐杆线虫,一种广泛用于遗传实验的线虫蠕虫。蠕虫在大约10天内变得瘫痪。挑战是寻找一种拯救他们从某些死亡的方式。“我们在Alex Parker的监督下,Julie Veriepe,Lead Sorfiger和Docatal Carture表示,我们对其在免疫系统中的作用进行了修改了另一种众所周知的作用。结果显着。她补充说,“患有TIR-1基因突变引起的免疫缺陷导致的蠕虫具有更好的健康,并且瘫痪远低于瘫痪。
这项研究突出了以前涉嫌涉嫌机制:即使C.秀丽隐杆线虫有一个非常基本的免疫系统,那么系统触发了对抗蠕虫自己的神经元的误导攻击。'蠕虫认为它具有病毒或细菌感染并发射免疫反应。但反应是有毒的,摧毁动物的运动神经元,'Alex Parker解释道。在与人们合作的同样的场景?最有可能的。人类相当于TIR-1基因 - SARM1-已证明对神经系统的完整性至关重要。研究人员认为信号通路对于与ALS相关的所有基因相同。这使得TiR-1蛋白(或人类中的SARM1)用于发育药物的优异治疗靶标。SARM1尤为重要,因为它是众所周知的激酶活化过程的一部分,其可以被现有的药物阻挡。
Alex Parker的团队已经积极测试以前经过美国食品和药物管理局批准的药物,以治疗这种疾病作为类风湿性关节炎,看他们是否与ALS合作。然而,在找到固化或减缓进展的补救措施之前仍然存在障碍肌营养的外侧硬化。“在我们用蠕虫的研究中,我们知道动物生病,因为我们导致疾病。这使我们能够在蠕虫的生命中非常早期地管理治疗。但Als是一种衰老的疾病,通常出现在55岁左右的人类中。如果潜在的药物,如果潜在的药物将有效,如果症状的出现后才会给出。但我们清楚地证明,阻止这种关键的蛋白质在这虫中抑制了这种疾病的进步,'Alex Parker得出结论。
进一步探索









用户评论