新的测量显示干细胞治疗视网膜变性之间的区别
生长两种类型的干细胞在“三维文化”和测量他们产生视网膜细胞的能力,团队领导,圣裘德儿童研究医院的研究人员发现了一种细胞类型更擅长产生视网膜细胞。
这项研究不仅揭示了干细胞类型可能是更好的治疗视网膜变性,但它也演示了一个标准化的方法量化等不同的干细胞疗法的有效性。
这项研究是由迈克尔•戴尔博士,一位圣裘德发育神经生物学和霍华德·休斯医学研究所研究员。这项研究结果发表在7月2日出版的《华尔街日报》细胞干细胞。
干细胞是未成熟的细胞,可以分化成更专门的细胞在体内。在早期的临床试验中,研究人员正在测试是否干细胞可以分化成细胞来取代那些缺陷和死亡疾病,如年龄相关性黄斑变性、视网膜色素变性和黄斑变性的疾病。这样的变性是视力丧失的主要原因,影响超过1000万人在美国——比白内障和青光眼的总和。
尽管这类临床试验显示早期的承诺,有许多科学问题需要回答。“一个重要的问题是,它使不同的干细胞是从哪里来的,”戴尔说。“我们的研究试图探讨这个问题,也更多地了解这些干细胞的生物学”。
研究人员比较了两种类型的干细胞被称为“诱导多能干细胞”,这可以从成年细胞生成。他们比较的干细胞是fibroblast-derived细胞产生的皮肤,和那些来自成熟的眼睛视杆细胞。
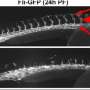
科学家先前认为诱导多能干细胞不能用成人的神经元没有引入突变,关闭一个关键调节基因p53。戴尔的实验室开发了一种新方法从神经元干细胞不需要p53失活。这种三维文化技术涉及到周围的神经元进行重组与正常视网膜神经元,创建一个更自然的环境产生干细胞的神经元。这种技术与更常见的文化技术不断增长的细胞层文化菜,这对于这些细胞不成功。一旦产生的干细胞,他们可以用来制作三维文化的视网膜细胞。
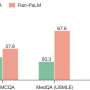
除了三维文化技术,研究人员也使用一组测量,称为STEM-RET,这使他们能够精确量化不同视网膜细胞在多成功产生视网膜细胞。STEM-RET分析表明rod-derived干细胞产生更多的视网膜细胞比纤维母细胞的干细胞。缺少一些fibroblast-derived视网膜细胞细胞类型需要全功能的视网膜。
戴尔和他的同事们还探讨了两种干细胞的生物学差异可以解释他们的差异产生视网膜细胞。具体地说,研究人员分析了不同的表观遗传控制两种类型的机器。这种细胞的表观遗传机制包括生物开关,控制细胞的基因。这些都是不同于遗传控制机器内置的DNA结构细胞的基因本身。
科学家认为不同的干细胞类型可能保留一组“表观遗传记忆”——独特的表观遗传开关,即使他们从成熟细胞重新编程。这种“记忆”影响干细胞如何产生不同的细胞类型。
在他们的视网膜细胞的分析,研究者发现一种表观遗传开关,叫做CTCF,它有助于rod-derived干细胞的表观遗传记忆。这种表观遗传开关,他们相信,可以扮演一个角色在杆干细胞上级的视网膜细胞来源。
Dyer说STEM-RET得分的干细胞标志着一个重大的进步在决定使用哪个干细胞在视网膜干细胞疗法。”一直是该领域的讨论如何规范的量化干细胞分化,”他说。“我们STEM-RET方法使标准化,这意味着实验室彼此能精确地比较他们的结果和不同的干细胞系可以相比。我们认为这个方法可以被广泛采用。”
这些干细胞表观遗传分析可能导致“表观遗传指纹”描述不同的干细胞类型。”这样的指纹会告诉研究人员干细胞系最有可能是有效的视网膜细胞、骨髓细胞或其他类型的成熟细胞治疗的目的,”戴尔说。
3 d技术和文化STEM-RET测量协议允许科学家操纵干细胞基因和药物发现方法来更好的重组细胞功能成熟细胞治疗使用。