研究人员发现在抗击感染时,如何在免疫系统如何产生癌症DNA突变

长期以来,由疾病或接触危险化学物质引起的慢性炎症一直与癌症有关,但这一过程究竟是如何发生的仍不清楚。
现在,慢性炎症可以导致癌症的精确机制被发现研究人员麻省理工学院的一项研究表明,这一进展可能会为预防未来的肿瘤提供更好的靶点。
在本周发布的论文中美国国家科学院院刊,研究人员揭示了一个电池如何化学战具代理商由免疫系统用于抵抗感染本身可以产生导致癌症的DNA突变。
据信,多种癌症中的一种癌症被炎症促进或促进。这些包括间皮瘤,一种由慢性暴露于石棉的炎症引起的肺癌,以及麻省理工学院的生物工程系的研究助理和炎症肠道疾病的患者的结肠癌。领导作者。
天生免疫反应
炎症是身体对入侵病原体或潜在有害刺激物的原生物反应的一部分。免疫系统用旨在中和的多种反应性分子攻击入侵者,包括过氧化氢,一氧化氮和次氯酸。
然而,这些分子也可以对感染部位周围的健康组织造成旁观性损伤:“外来病原体的存在激活免疫应答,这试图消除细菌,但在该过程中,它也损害了一些正常细胞,“Fedeles解释道。
以往的工作由Peter Dedon,Steven Tannenbaum,Gerald Wogan和James Fox--所有教授生物工程在MIT - 已经确定了在感染病原体幽参病病原体肝动晕的小鼠的发炎组织中称为5-氯结菌(5CLC)的DNA结构的病变或损伤部位。这种病变是正常DNA基础胞嘧啶的受损形式,是由反应性分子次氯酸 - 家庭漂白剂中的主要成分 - 由免疫系统产生。
John Essigmann,John Essigmann,威廉R.(1956年)和MIT遗留教授的遗留教授,MIT居民教授的遗留教授,危险,危险的损伤,损伤,5CLC的病灶。
“他们发现病变在DNA中非常持久,这意味着我们没有一个修复系统来清除它们,”Essigmann说。他补充说:“在我们的研究领域,持续性的病变,如果它们也具有诱变性,就是会引发癌症的病变。”
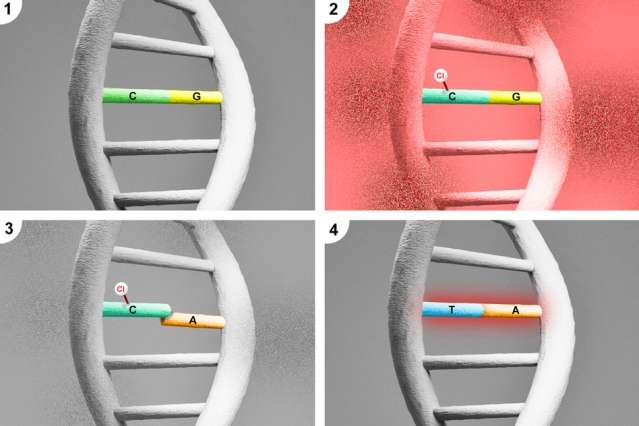
显影胃肠肿瘤的DNA测序显示出两种类型的突变:胞嘧啶(C)碱基转换为胸腺嘧啶(T)碱基,并且腺嘌呤(A)碱变为鸟嘌呤(G)碱基。由于5CLC尚未被研究作为潜在的致癌诱变,研究人员决定进一步调查病变,以揭示它,如果它确实致致致残。
使用先前在Essigmann的实验室开发的技术,研究人员首先将5Clc病变放在细菌病毒的基因组内的特定部位。然后他们将病毒复制在细胞内。
根据Essigmann的情况,研究人员发现,而不是始终将鸟嘌呤碱与鸟氨酸碱配对,而是将5%的腺嘌呤基座与excermann的时间相关的突变频率搭配。
损坏的DNA
调查结果表明免疫系统当被感染触发时,它会在患处点燃次氯酸,破坏周围健康组织DNA中的胞嘧啶。这种损伤导致一些胞嘧啶变成5ClC。
此外,研究人员还假设,次氯酸也会损害核苷酸库中的胞嘧啶,细胞将核苷酸用作存储库,这些核苷酸将成为复制细胞DNA的一部分,Essigmann说。“所以5ClC首先在基因组DNA中形成,其次它可以在核苷酸池中形成,这意味着池中的核苷酸本身具有诱变作用,”他解释说。“这个设想最好地解释了詹姆斯·福克斯和他在麻省理工学院的同事们对胃肠道癌症的研究。”
为了确认5CLC在人体DNA中致致诱变,研究人员将含有病变的基因组与各种不同类型的聚合酶一起复制,该酶组装DNA的酶,包括人聚合酶。“在所有情况下,我们发现5CLC是致突变的,并导致细胞内看到的相同类型的突变,”Fedeles说。“这给了我们确信这种现象实际上发生在含有高水平5Clc的人体细胞中。”
更重要的是,5CLC的C-TO-T突变特征是非常常见的,并且存在于50%以上的诱变“签名”或与癌症肿瘤相关的DNA突变的模式。“我们相信在背景下炎症诱导DNA的损伤,其中许多C对T突变可能是由5Clc引起的,可能与其他类型的突变相关,作为这些突变签名的一部分,“Fedeles说。
加州大学河滨分校(University of California at Riverside)化学系首席研究员王银生(音)没有参与这项研究,他说,这篇论文提供了一种新的机制联系慢性炎症和癌症发展。“随着生化,遗传和结构生物学方法的组合,研究人员发现,5-氯霉素在DNA复制期间无内在错误分量,它可能导致C-TO-T突变的显着频率,这是一种突变王说,在人类癌症中经常观察到。
患有患者组织样本的研究炎症性肠病发现的5Clc水平显着,Fedeles补充道。通过将这些级别与他的团队的调查结果进行比较,研究人员预测,诸如荣誉的本杰明F.特朗普奖,该研究人员预测病变的积累将增加高达30倍的细胞的突变率高达30倍在2015年的Aspen癌症会议上进行了研究。
Fedeles说,研究人员现在计划进行进一步的研究来证实他们的预测。
进一步探索
这个故事被重新发布由麻省理工学院新闻(web.mit.edu/newsoffice/),一个涵盖麻省理工学院研究、创新和教学新闻的热门网站。












用户评论