iPS细胞发现治疗肌肉疾病的药物靶点
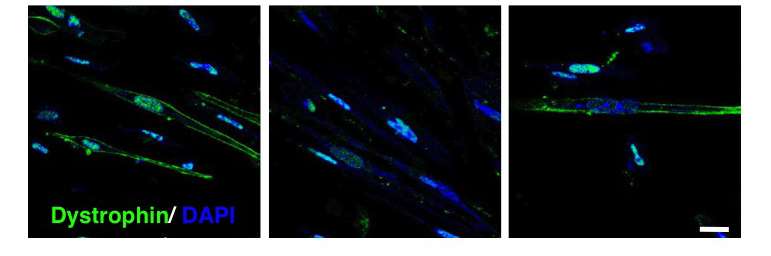
Duchenne肌营养不良(DMD)是一种肌肉疾病,表现出幼儿早期症状,并导致进步萎缩和最终死亡。在治疗方面几乎没有,部分原因是对DMD如何发展的理解差,尽管众所周知,蛋白质营养蛋白的异常表达处于故障。
通常,研究DMD开发,患者肌肉,细胞发展成肌细胞,用于研究DMD的发展。但由于DMD分期不同,患者的细胞不适合研究早期DMD发展及预防措施。为了克服这个问题,樱井秀敏,CiRA的高级讲师,和他的团队,与京都大学前沿医学科学研究所合作,设计了一个模型,重新编程成纤维细胞,使其分化为完整的肌肉细胞的早期阶段。
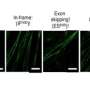
该方法首先将病人的细胞重新编程为诱导多能干细胞(iPS),然后引入一种将iPS细胞分化为肌肉细胞的基因。CiRA研究人员Emi Shoji说:“我们的模型允许我们使用相同的基因背景来研究发病的早期阶段,这在过去是不可能的。科学报告这为DMD开发提供了新的见解。
肌肉收缩取决于钙离子(Ca2+)流入细胞。然而,过多的内流会导致细胞功能障碍或死亡,这被认为是引起DMD的根本原因。Shoji说:“为了准确评估Ca2+内流如何导致DMD致病级联,评估完整细胞是至关重要的。”因此,她通过电刺激他们的模型来模拟肌肉细胞的收缩,发现DMD患者的细胞内流明显增加。进一步的研究认为Ca2+离子通过瞬时受体电位(TRP)通道进入细胞。这一观察结果与其他模型一致,为DMD的治疗提供了明确的药物靶点。更重要的是,它应该让科学家发现可以在早期发展中对抗DMD的药物。“色氨酸通道以前已经确定。但是因为我们的模型使用的是患者来源的hiPS细胞,所以我们有可能找到治疗DMD的新药,”樱井说。
进一步探索





用户评论