新的研究提供炎症和结肠癌转移之间的联系
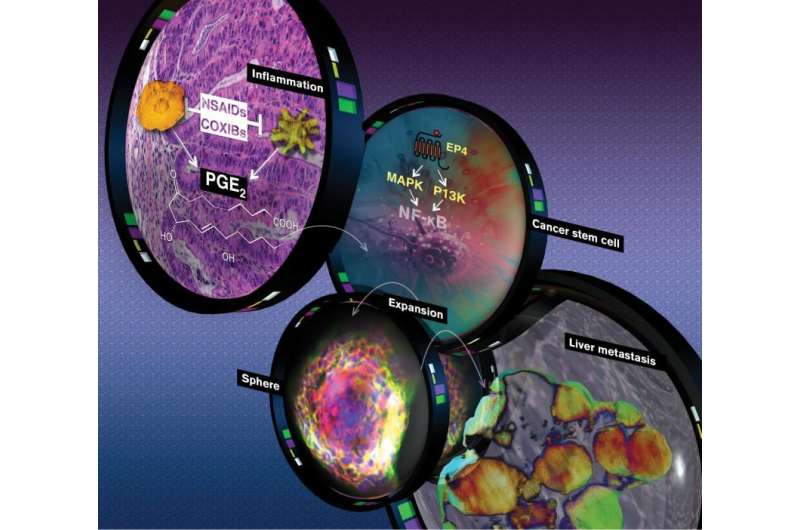
新亚利桑那州立大学研究学习由生物选择研究所执行董事Raymond Dubois,M.D.,Ph.D,首次确定了炎症如何触发结肠癌细胞传播到其他器官或转移的细节。
调查结果将使研究人员识别用于预防和治疗结肠癌的新药物目标。Dubois,领导者结直肠癌研究超过二十年,一直在探索慢性炎症和癌症之间的危险因素,包括结肠直肠癌。
“我们很久都知道服用阿司匹林或其他抗炎药(称为非甾体抗炎药或NSAIDs)的简单的东西对降低结直肠癌的风险有益,”Dubois说。“但是在长时间服用时,非阿司匹林NSAID可能会导致严重的心血管副作用,所以我们需要发现更好的药物目标。这项研究指出了正确的方向。”
结果可能意味着更有效的结直肠癌处理和筛选方法的新希望。目前,治疗后五年内近一半的晚期结直肠癌死亡。一种原因可能是癌症变得更加化疗,但其他证据支持炎症和炎症介质在肿瘤转移中的作用。
研究团队能够展示结肠癌肿瘤如何使用炎症调解剂来扩大其癌症的宿主干细胞为了寻找其他器官。它们显示出促炎介质前列腺素E2和增加的结肠直肠癌干细胞之间的直接联系。
癌症是由许多不同类型的细胞组成的遗传动物园。这些细胞中的一些称为癌症干细胞(CSCs),被认为是肿瘤引发,生长,复发和复发的原因。
前列腺素E2是最丰富的促炎生物活性脂肪,或脂质,在结肠,肺癌,乳腺癌,头部和颈部癌症中发现。当在癌症中发现高水平的PGE2时,它通常表明预后差。
“PGE2的正常角色是当你做一些像剪指的东西时会来救援,”Dubois说。“它吸引了身体的免疫细胞并刺激治愈伤口部位的途径。PGE2的水平上升,然后在愈合伤口的几天内下降。
但在癌症中,细胞长期地保持PGE2,所以它就像这种伤口过程中从未愈合。在这样做时,它产生促进癌症进展和转移性传播的这些癌症干细胞。“
Dubois的研究团队证明,当PGE2在癌细胞表面的表面上与其受体结合时,PGE受体4或EP4的受体结合,它触发了用于癌症干细胞的信号级联,以更新,分化,最终对化疗抵抗力。
它好像原始癌症肿瘤细胞饥饿并在结肠的供应物上运行低,通过制作PGE2来欺骗其主体,以发出新的干细胞的帮助信号,以建立救生筏并在整个中找到安全港身体再次繁殖。
Dubois能够在鼠标模型中表现出结直肠癌的模型,添加PGE2增加了CSC和整体肿瘤负担的数量,肝脏是结直肠癌首次传播的素器靶标的靶标。
“我们使用利用人类组织和小鼠模型的方法组合来完成我们的研究,”Dubois说。“我们从人结肠癌中取样,然后净化癌症干细胞人口。当我们用PGE2对待这些干细胞时,我们发现它们比我们不用PGE2对待的细胞比细胞更多的转移倍增。“
此外,在人结肠癌组织标本中也可以看到升高的PGE2水平和增加的CSC数量。
此外,当通过添加抑制与EP4受体结合的药物来阻断PGE2信号传导时,它减少了息肉和CSC的数量,并阻断了肝脏转移。
本文是第一个显示撞击PGE2对CSCS对肝脏的蔓延的影响。随着新的证明,Dubois对未来的研究很乐观。
“现在,如果我们只能瞄准并消除人的干细胞结肠癌,我们可以制定一种新的治疗结肠直肠的治疗方法癌症并改善结果,“Dubois说。
Dubois希望人体临床试验可以在合理的时间内启动,以表明新药物目标策略的有效性。
调查结果显示在期刊上的最新问题中胃肠病学。









用户评论