研究小组报告了个体化细胞治疗后多发性骨髓瘤的持续缓解
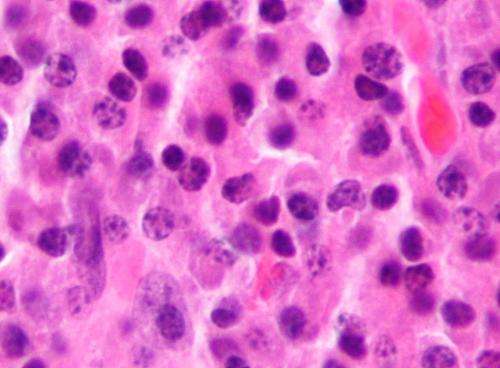
一名多发性骨髓瘤患者在接受了宾夕法尼亚大学一个研究小组开发的名为CTL019的研究性个性化细胞疗法后,其癌症在9种不同的治疗方案后停止了反应,并获得了完全缓解。试验性治疗与化疗和自体干细胞移植相结合——这是一种新的策略,旨在靶向并杀死产生骨髓瘤细胞的细胞。
该研究小组的研究结果发表在今天的《柳叶刀》杂志上的一份病例报告中新英格兰医学杂志.在接受治疗之前,患者在诊断后的5年里已经接受了9种不同的治疗方案,包括之前的自体治疗干细胞移植她的病情只控制了几个月。她的骨髓里几乎全是癌细胞当她走进书房时。在接受工程细胞注入130天后,测试没有显示任何疾病的证据。该患者是该试验中第一个接受治疗的患者,在接受治疗12个多月后仍处于缓解状态。
这份新报告扩展了2015年6月美国临床肿瘤学会会议上提出的关于第一批5名接受CTL019治疗的骨髓瘤患者的数据,CTL019在2010年开始的白血病试验中进行了测试。现在,宾夕法尼亚大学的研究团队也报告了骨髓瘤试验的总体进展:在10名接受治疗的患者中,有6名患者没有进展,尽管有2名患者最近才接受治疗。
“我们对这位患者的反应感到非常满意,”该研究的共同主要作者、宾夕法尼亚大学阿布拉姆森癌症中心和佩雷尔曼医学院血液学/肿瘤学助理教授阿尔弗雷德·加福尔医学博士说。“我们相信她的CTL019细胞起了作用,因为考虑到这位患者几年前对第一次移植的反应非常短暂,我们不会期望仅通过移植就有如此持久的缓解。”
CTL019从每个患者自己的T细胞开始,通过类似于透析的程序收集。然后,这些细胞被重新编程,以捕猎和潜在的杀戮癌症细胞在病人的身体里。参加该方法治疗急性淋巴细胞白血病(ALL)、慢性淋巴细胞白血病(CLL)和非霍奇金淋巴瘤(NHL)试验的患者,在接受新工程细胞输注之前,通常要接受淋巴消耗化疗。改良的T细胞含有一种被称为嵌合抗原受体(CAR)的蛋白质,它被设计用来靶向B细胞表面的CD19蛋白,包括几种类型的白血病和淋巴瘤的特征癌B细胞。
该团队设计了一种不同的方法来研究骨髓瘤的治疗,加入了患者自己的输液干细胞以及他们的淋巴消耗化疗(美法兰),然后在大约两周后输注CTL019。尽管骨髓瘤像白血病和淋巴瘤一样,是一种涉及白细胞被称为淋巴细胞,骨髓瘤细胞它们的表面传统上不表达CD19,因为它们来自最成熟的淋巴细胞——浆细胞。
该研究的资深作者Edward Stadtmauer医学博士说:“对于CD19靶向治疗是否对这种疾病有效有一些怀疑,因为几乎所有这些患者的癌变浆细胞都不表达CD19。”Edward Stadtmauer是血液恶性肿瘤的主任,也是宾夕法尼亚大学艾布拉姆森癌症中心和佩雷尔曼医学院的血液学/肿瘤学教授。“因为有数据表明,可能的干细胞可能是cd19阳性的,我们的假设是,我们可能能够设计一种针对这些细胞早期前体的治疗方法。”
在接受CTL019之前,患者经历了移植相关的副作用,包括中性粒细胞减少症和血小板减少症、恶心、发烧和感染。在接受工程细胞后,她没有出现发烧或其他细胞因子释放综合征(CRS)的症状,这种症状在接受CTL019治疗的其他患者中也有观察到。
该研究的资金部分由诺华公司提供,由美国国立卫生研究院(K12CA076931, K08CA166039,和5R01CA165206)和征服癌症基金会提供资助。
编者按:宾夕法尼亚大学已将本试验涉及的技术授权给诺华。参与这些试验的一些科学家是这些技术的发明者。由于与诺华的授权关系,宾夕法尼亚大学获得了巨大的经济利益,这些发明者已经获得了经济利益,或在未来可能获得经济利益。更多披露信息见论文。
由于CTL019是一种试验性的治疗方法,其安全性和有效性尚未确定。只有通过仔细控制和监测的临床试验,才能获得研究性疗法。这些试验旨在更好地了解治疗的潜在好处和风险。CTL019输注后,细胞因子释放综合征(CRS)可发生细胞在患者体内被激活并繁殖导致细胞因子的释放。在CRS,病人通常会出现不同程度的流感样症状,包括高热、恶心、肌肉疼痛,在某些情况下还会出现低血压和呼吸困难。CRS严重程度与疾病负担相关。此外,CRS也可以发生在其他非car治疗环境中,包括一些单克隆抗体。