凝血蛋白触发了对大脑的免疫攻击
格莱斯顿研究所的一项新研究表明,大脑中的一滴血足以激活类似于多发性硬化症(MS)的自身免疫反应。这是第一次证明,在健康的大脑中输入血液足以导致外周免疫细胞进入大脑,进而导致大脑损伤。
一个中断血-脑屏障(BBB)允许血液蛋白质泄漏到大脑,是多发性硬化症(一种大脑和脊髓的致残性自身免疫性疾病)的关键特征。然而,目前尚不清楚BBB的中断是否导致了自身免疫反应或者由此产生的结果。
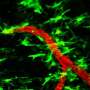
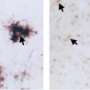
在目前的研究中,发表在自然通讯在美国,科学家们创造了一种新的动物疾病模型,以确定血脑屏障渗漏是否会导致自身免疫。他们发现,只要向大脑中注入一滴血,就会引发大脑的免疫反应,引发连锁反应,导致炎症和髓磷脂损伤。髓磷脂是保护大脑神经纤维的鞘,是多发性硬化症损伤的主要部位。此外,科学家们能够确定血液中的一种特定蛋白质,即凝血因子纤维蛋白原,是致病过程的触发点。
“这些发现提供了一种全新的方式来思考免疫系统如何攻击大脑——它把血液放在了疾病发生和发展的驾驶位置上,”资深作者Katerina Akassoglou博士说,她是格拉德斯通研究所的高级研究员,也是加州大学旧金山分校的神经学教授。“这为针对自身免疫过程上游凝血因子的新型疗法开辟了可能性。”
纤维蛋白原激活了被称为小胶质细胞的大脑免疫细胞,并使它们发出信号,召唤身体其他部位的外周免疫细胞到大脑。当这些外周免疫细胞——巨噬细胞和T细胞——进入大脑时,它们攻击髓磷脂。
“我们的研究结果提供了血液促进T细胞对抗大脑反应的第一个证据,”Gladstone研究所的工作人员、第一作者Jae Kyu Ryu博士说。“我们不仅确认了大脑中血液的存在会招募周围免疫细胞到该区域,这足以导致髓磷脂破坏,我们还确定了纤维蛋白原是驱动这一过程的关键蛋白质。”
为了证实他们的发现,科学家们删除了小胶质细胞上的纤维蛋白原受体(补体受体3或CD11b/CD18),从而阻止纤维蛋白原激活细胞。抑制这种相互作用阻断了自身免疫过程,阻止小胶质细胞向外周发送信号免疫细胞避免髓磷脂损伤和炎症。研究人员现在正试图使用生物和小分子方法阻断纤维蛋白原,作为抑制针对大脑的自身免疫的潜在新疗法,抑制小胶质细胞和T细胞引起的炎症。
加州大学旧金山分校神经学教授、论文合著者Scott Zamvil博士说:“这些发现质疑了一个长期以来的模式,即髓髓蛋白特异性T细胞通过激活小胶质细胞和脑巨噬细胞引发大脑炎症。”“这项研究表明,原来的范式也可能发生相反的情况。也就是说,小胶质细胞和脑巨噬细胞的初始激活可能激活T细胞。”
科学家们说,拥有一个血液诱导的大脑炎症模型是一个有价值的工具,因为它可以用来筛选新药。这些机制不仅可能发生在自身免疫性疾病中,也可能发生在其他涉及炎症或血脑屏障破裂的脑疾病中,包括创伤性脑屏障大脑受伤、中风、阿尔茨海默氏症和其他痴呆症。