化学诺贝尔DNA研究为对抗癌症的新方法奠定了基础
我们的细胞每天都会对编码基因的DNA造成大量损害。我们需要不断的努力来跟上DNA的失修——如果我们的细胞不费事去修复它,我们可能无法生存。DNA损伤修复途径是人类基因组的重要保障。
这2015诺贝尔诺贝尔在化学中他们因研究出细胞用来修复DNA损伤的分子机制而获得该奖项。在他们的基础研究中,Tomas Lindahl.那保罗莫里希和Aziz Sancar.每次缩小一块DNA修复拼图。
他们为研究的研究奠定了框架,即许多基本和翻译科学家正在扩展试图破解癌症。具有讽刺意味的是,我们发现方法可以将DNA修复系统转化为癌症细胞,该细胞通常首先从DNA损伤中出现。
DNA围困
DNA由四个简单的字母组成,或核苷酸,A,T,C和G.当组合时,这些核苷酸形成遗传密码。有大约30,000个基因在人类基因组中。
每次细胞生长和分裂时,每一个基因都需要忠实地复制到下一代细胞中。DNA复制的过程不断受到来自内部和外部的DNA损伤来源的威胁。有环境来源,如来自地球的氡或来自太阳的紫外线。也可能只是细胞正常生长和分裂时发生的一个错误。一些研究估计单个细胞可以经历一天内发生数千起DNA损伤事件。
接下来的问题是:细胞如何修复这些损伤?或者更令人担忧的是,如果细胞不能修复损伤会发生什么?
一个完整的工具箱,可以处理损坏
为了抵消DNA损伤的日常冲击,哺乳动物细胞已经进化了许多复杂的机制,不仅识别DNA损伤,而且修复并恢复原始遗传序列。
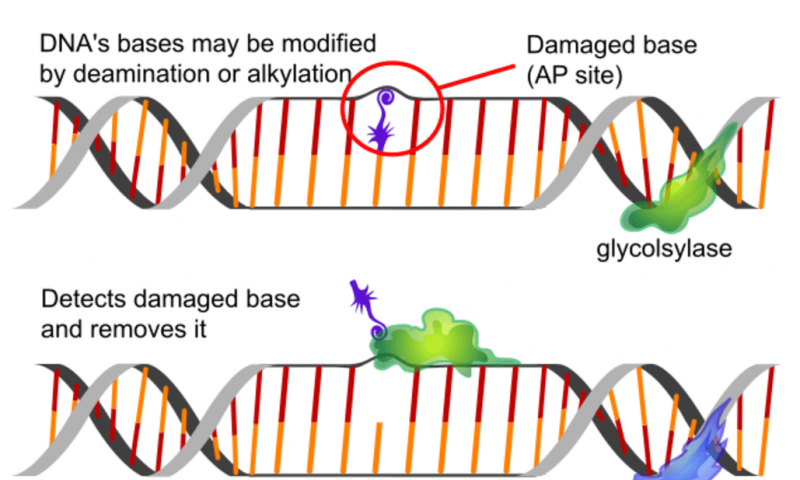
考虑一个改变字母n的拼写错误,导致“咧嘴”变成“严峻”。单个错字现在现在改变了这个词的整个含义。当核苷酸不正确的核苷酸取代右侧的位置时,它在遗传密码的“单词”中工作。DNA损伤修复酶的功能类似于橡皮擦将突变部门恢复到原来的N.
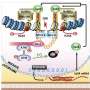
在DNA损伤之后,细胞必须首先识别损坏,然后提醒系统存在问题。然后,识别机制激活各种因素以停止细胞生长,直到损坏已经修复。如果事情过得太远,额外的因素已经准备好并准备诱导细胞死亡。
这是思考DNA损伤响应途径的最基本方式,作为一种简单的事件链。当然,这是一个更复杂,复杂的检查和余额网络,以确保DNA损伤不仅认识而且清楚地确定,以确保招募正确的因素来修复病变。
就像房主不希望电工来修补漏水的屋顶一样,DNA“拼写错误”也不应该通过用于修复DNA双链断裂的机制来修复。因此,检测哪一种特定的遗传损伤是DNA损伤反应途径中最早也是最关键的步骤之一。
很难说到底有多少DNA损伤反应“传感器”,或者它们到底是谁,但这是该领域正在积极研究的东西。同样地,尽管我们所知道的DNA损伤修复途径的数量自从诺贝尔奖的开创性工作完成后并没有必然增加,但我们理解的复杂性却有所增加。
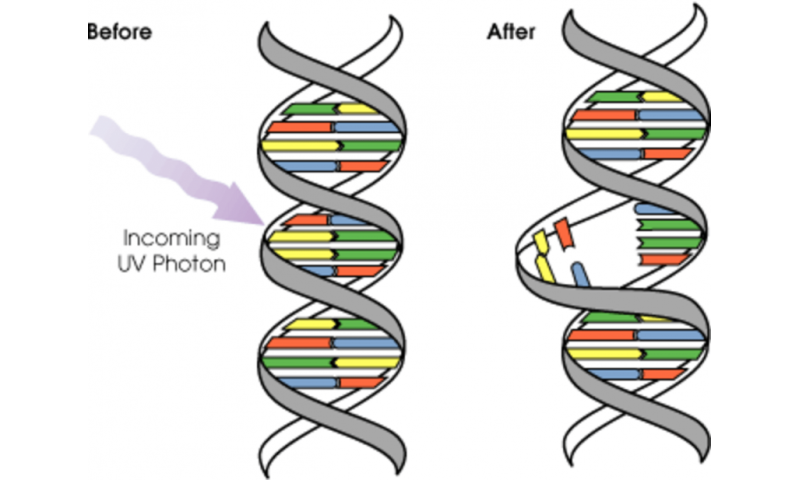
如果修复过程本身坏了怎么办?
在有限的容量中,突变实际上有助于进化。自然选择必须发生变化,因此这些DNA突变是达尔文进化理论的重要因素。然而,祝福也可能是一种诅咒。
必需基因的突变可以导致死亡甚至在我们进入这个世界之前。然而,非必需基因的突变可能要到生命的后期才会显现出来。当这些突变持续存在——或者更糟的是,积累起来——就会导致基因组不稳定。这是癌细胞的一个特征。
然后,您可以想象,DNA损伤响应途径的组分中的单一突变可能导致DNA损伤,基因组不稳定性的积累,并最终进入癌症。这是真的,我们经常在癌症中造成DNA损伤反应途径的突变。完全解读这些途径工作对于我们不仅是癌症的理解至关重要,也是我们如何利用这些途径来实际治疗这种疾病。
利用修复系统来达到我们的目的
这些损伤修复途径对于防止遗传病变的积累是必不可少的,并且最终抑制癌症的进展。有没有办法我们可以利用系统,将其推过边缘并导致不需要的单元格,而不仅仅是为了死亡而是死亡?
为此,研究人员在工作中努力尝试进一步定义调节DNA损伤反应的细节。其他人正在努力确定我们可以治疗的因素。
一旦DNA损伤反应途径已经被突变灭活,就以它为目标似乎违反直觉。但这种方法也有其优势。
一般来说,当基因突变使修复的一个分支失活时,细胞会试图通过使用另一种类型的修复来进行补偿,只是为了保持细胞的活力。你是愿意打电话给电工,希望他能把漏水的屋顶修好,还是冒着整个屋顶塌下来砸到你身上的风险?
该单元选择备用机制以尝试解决损坏。通常,这导致修复不足和收购额外突变,加以基因组不稳定性和癌症进展。
我们希望消除备用机制 - 将电工送出城镇。研究表明,当一种类型的修复机制因遗传突变而灭绝,并且治疗上灭活备用机制时,癌细胞死亡。同样,如果我们将诱导特定类型的损伤的药物组合,然后灭活特定的修复途径,细胞死亡。临床科学家已经证明,这可能导致引发患者的肿瘤回归这一领域的研究激增。
针对端粒
我的实验室想要了解DNA损伤反应是如何在端粒DNA上被调控的。
端粒是一个重复的DNA序列,覆盖了每个人类染色体的末端。端粒起到屏障的作用,保护人类基因组免于降解和/或整个染色体的融合。
每次一个细胞分裂时,这个屏障的一部分都会丢失;随着时间的推移,缩短端粒损害了基因组的稳定性。为避免对基因组损伤,统治性短端粒体向细胞发送信号以停止生长或诱导细胞死亡。
然而,癌细胞已经进化了克服逐步端粒缩短和绕过这种生长阻止的机制。换句话说,它们突出了正常的常规,分割和生长,同时避免了端粒缩短的通常步骤,最终导致正常细胞死亡。他们反击端粒缩短和促进端粒伸长的一种方式是激活端粒选择性延长途径(ALT)。

这ALT机制活跃在10% - -15%的所有的人类癌症。这种发病率在一些最具侵略性形式的人类癌症中飙升至约60%,包括骨肉瘤和胶质母细胞瘤。这些癌症往往抵抗普通的治疗策略,并且没有特别靶向ALT途径的疗法。
在我的实验室中,我们专注于其中一个分子,它在第一位置感测DNA损伤,ATR激酶。我们发现,防止其作业导致端粒的重组减少,并且染色体末端的端粒损失增加,表明ALT活性的缺陷。
也许最重要的是ATR抑制导致了灾难性的细胞分裂和细胞死亡在Alt阳性癌症中细胞但对非癌细胞系影响不大。
这些研究可能允许我们将ATR抑制剂驱动到临床前的发展中,并具有改善治疗一些最具侵略性形式的人类癌症的治疗策略的最终目标。
这种转译研究建立在我们最新的诺贝尔化学奖得主的工作框架上。他们的基础研究被证明是靶向癌症(并有望治疗癌症)新方法的基础。
进一步探索
这个故事发表了礼貌谈话(在创作共性/无衍生品下)。![]()











用户评论