研究人员描述了早衰症背后的机制
早衰症是一种过早衰老的疾病,是维也纳大学和维也纳医科大学Max F. Perutz实验室Roland Foisner团队的研究重点。患有早衰症的儿童平均在14到15岁时死亡,通常死于心脏病和中风。到目前为止,这种疾病还没有治愈的方法,尽管研究人员发现了这种疾病背后的异常蛋白质——孕激素,但它导致加速衰老的确切方式仍然不清楚。在他们最新出版的基因与发展, Roland Foisner和他的团队描述了早衰症背后一个未知的机制,这可能为治疗提供新的方法。
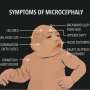
孩子遭受儿童的早衰症出生时是正常的,但从1岁到2岁,他们的疾病在某些方面开始类似于过早衰老。因此,当他们进入青少年时期时,就会出现典型的与年龄有关的疾病,如骨质疏松、关节僵硬和严重的心血管疾病。最后,许多人在20多岁之前死于中风和心脏病。目前,还没有治愈早衰症的方法。患者可以使用一种叫做FTIs(法尼酰基转移酶抑制剂)的药物进行治疗,这种药物最初是为治疗癌症而开发的。这些药物改善了疾病的某些方面,如骨骼结构、动脉硬化,并将估计寿命至少延长1.6年。
Progerin:导致早衰症的蛋白质
Progerin是一种存在于早衰症细胞中浓度极高的蛋白质,被认为是导致该疾病许多特征的原因。它是lamin a的突变体,lamin a是一种对细胞核的稳定性至关重要的蛋白质,参与了许多基本的核功能。progerin是如何发挥作用的,这是Roland Foisner和他的团队在Max F. Perutz实验室的研究兴趣。Max F. Perutz实验室是维也纳大学和维也纳医科大学的合资企业。他们研究了核层膜的分子功能及其突变形式,如孕激素和相关疾病。
“几年前,我们和其他人发现早衰症细胞的LAP2α含量比正常细胞少得多。LAP2α是一种蛋白质,与层蛋白a相互作用,调节细胞增殖,产生新细胞的过程。有趣的是,LAP2α水平在正常衰老过程中也会下降,”维也纳医科大学医学生物化学系副主任Roland Foisner解释道。在早衰症研究基金会创新奖的支持下,高级博士后Thomas Dechat和博士生Sandra Vidak与美国国立卫生研究院国家癌症研究所的Tom Misteli合作开发了一种细胞系,可以在实验室中研究早衰症背后的分子机制。Vidak说:“与正常细胞相比,产生孕激素的细胞LAP2α水平非常低。而当我们重新引入LAP2α时,我们可以完全挽救早衰细胞的增殖缺陷。同样的情况也发生在患者样本的细胞中。”
LAP2α与孕激素的相互作用
进一步的实验揭示了一个真正的惊喜:LAP2α在早衰症细胞中的功能与正常细胞有很大的不同。通常它结合在一个不同的核池的层蛋白a和减缓增殖,所以低LAP2α水平导致过度增殖。但在早衰症中,情况恰恰相反,细胞增殖速度慢得多,过早进入细胞老化过程。原因是早衰症细胞没有核层蛋白A池。这提示LAP2α在早衰症细胞中发挥作用的途径不同。最后,来自之前实验的数据给了研究人员解决这个难题的线索。“细胞被结构上支持它们的物质所包围。它被称为细胞外基质,简称ECM。此前有报道称,孕激素会对ECM蛋白的产生产生负面影响,导致细胞环境被破坏,增殖速度变慢。现在我们将其与低LAP2α水平联系起来当我们将LAP2α重新引入早衰症时细胞它们再次产生正常的ECM,并正常增殖,没有进入细胞衰老过程,”Vidak描述了她的发现。
该研究深入了解了为什么以及如何损害ECM蛋白的产生和正常增殖,为开发治疗早衰症更具体的治疗策略开辟了新的途径。随着过早衰老的疾病在许多方面与正常衰老相似的情况下,研究结果也可对正常衰老过程中的细胞过程作出结论。
该研究由早衰症研究基金会和奥地利科学基金FWF资助。桑德拉·维达克(Sandra Vidak)是一名博士生,参加了fwf资助的mpl“细胞信号分子机制”博士项目。
进一步探索











用户评论