研究将RNA剪接的特定变化与乳腺癌导致连接
研究人员已经发现了可能在正常乳腺细胞转化为肿瘤过程中发挥作用的细胞变化。针对这些变化可能会导致某些类型的乳腺癌的治疗。
在今天发表的工作中分子细胞,艾德里安教授领导的研究小组报告在冷泉港实验室(3)分析overexpressing促进蛋白质的影响称为SRSF1乳腺癌的细胞模型和在人类乳腺肿瘤,发现变化,可以负责SRSF1引起癌症的能力。
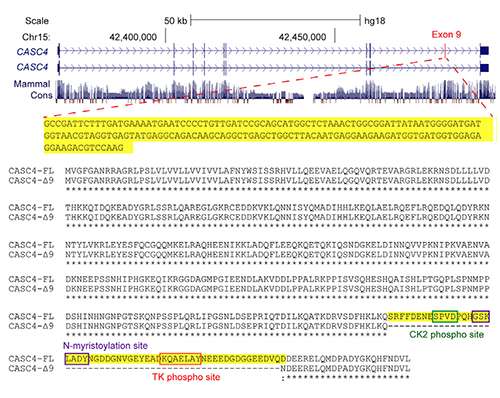
SRSF1是A.拼接因子,一种在基因产生蛋白质的过程中起关键作用的蛋白质。像SRSF1这样的剪接因子有助于编辑从基因中复制的编码“信息”。这些基因信息的副本被称为转录本,由RNA构成。剪接字面意思是剪去信息中不编码蛋白质的部分,称为内含子;它们将信息的其余部分(称为外显子)粘贴在一起,这些外显子确实编码蛋白质。
SRSF1和其他拼接因子也可以指导一个相关的过程可变剪接——一个基因的不同外显子的混合和匹配,当这些外显子拼接在一起时,就会产生单一蛋白质的变体,这些变体通常具有非常不同的功能属性。
“很久以前,我们和其他人发现,在各种癌症中,剪接蛋白质的水平发生了改变,”Krainer说。他说:“以前的工作表明,在癌症的背景下,剪接有很多变化。”
SRSF1以前显示为癌蛋白,即癌症中涉及的蛋白质。当它过度表达时,它可以帮助将正常细胞转化为肿瘤细胞。Krainer决定检查其在乳腺癌中的作用“因为我们看到乳腺肿瘤中SRSF1频繁过表达,”他说。
实验由Olga Anczukow和马丁·阿克曼,co-first新论文的作者,其他同事在报告中实验室,和他们的合作者在苏黎世ETH演示了如何SRSF1超表达的乳腺癌细胞模型,导致细胞RNA的变化产生的消息。这使得研究小组能够精确定位SRSF1调控的剪接靶点,并让他们看到这些细胞中与SRSF1相关的变化。
该团队确定并验证了SRSF1监管的数百个替代剪接事件。他们还研究了来自癌症基因组图集的数据,鉴定了与人乳腺肿瘤中的SRSF1过表达相关的替代剪接事件。“我们特别注意在所有这些不同的数据集之间重叠的潜在目标,因为它是一种缩小或给出可能发挥重要作用的目标的更高优先级的方式,”Anczuków解释道。
基于乳腺癌细胞系和人类的SRSF1过表达数据之间的重叠乳腺肿瘤,研究人员鉴定了一种称为Casc4的候选基因。过表达一种替代的Casc4蛋白的拼写形式部分地模仿过表达SRSF1的效果,表明Casc4有助于SRSF1的致癌作用。Krainer表示,CASC4可能只是解释SRSF1引起癌症能力的众多目标之一,而几个目标可能与音乐会行事,以产生与SRSF1过度表达相关的所有致癌变化。
识别由SRSF1和其他剪接因子引起的关键致癌替代剪接事件可能导致潜在的治疗靶标乳腺癌。“如果发现特定的变化在肿瘤维护中真的至关重要,那么我们可以开发恢复正常拼接模式的疗法,”克当克斯说。“这可能取决于少数,理想情况下是一个,但也许几个关键的目标是肿瘤真的依赖的。”
进一步探索











用户评论