研究停止了晚期犬X型X型视网膜炎粒子炎的视力丧失
三年前,宾夕法尼亚大学(University of Pennsylvania)的一个研究小组宣布,他们已经治愈了狗的x -连锁色盲性视网膜炎。现在他们已经证明,即使在一半或更多受影响的感光细胞被破坏后进行治疗,他们也可以长期治愈这种犬类疾病。
由于这种疾病对人类的影响与对狗的影响几乎相同,研究结果表明,这种治疗方法对人类可能是有效和持久的,并可能为人类临床试验之前的安全性研究奠定基础。
“2012年的研究表明基因治疗如果用作预防性治疗,或者在宾夕法尼亚州兽医学院培养了细胞死亡后止血后介入了细胞死亡后的权利。“这显然是非常令人鼓舞的”眼科的威廉A.Beltran,联合主教和副教授。但现在我们进一步走了,表明即使在中期和晚期疾病中开始,治疗也持久且有效。“
“这是一个非常严重的疾病,在人类的前两十年的生命中,潘恩·佩尔布尔曼医学院的Scheie Eye Institute of The-Hymology的artur V.Cideciyan,Cidecie and and Research教授。“因为狗中的疾病进展与人类的进展相匹配,这使我们对翻译这些结果最终对人类的进展提供了很多信心。”
这项工作由贝尔川和西德西扬、沙伊大学的眼科教授塞缪尔·g·雅各布森(Samuel G. Jacobson),以及论文的高级作者、宾夕法尼亚大学兽医学院(Penn Vet)的医学遗传学和眼科教授古斯塔沃·d·阿吉雷(Gustavo D. Aguirre)密切合作完成。宾夕法尼亚大学的研究人员还长期与佛罗里达大学的科学家合作,该大学的科学家由威廉豪斯沃思(William Hauswirth)领导,他是医学院的Rybaczki-Bullard眼科教授。
他们的研究发表在国家科学院的诉讼程序。
x -连锁视网膜色素变性(XLRP)主要是由RPGR基因突变引起的,导致从年轻时开始的进行性视力丧失。因为这是一种X染色体连锁的隐性疾病,它主要影响男孩和男人。这是一种最常见的遗传性视网膜疾病。
虽然严格研究,但关于RPGR的功能很少。据信在连接纤毛的功能中发挥作用,分别存在于杆和锥形细胞中存在的结构,感光体分别涉及昏暗的光和亮光的视觉。
在XLRP中,这些感光细胞逐渐退化并死亡。为了对抗这种效应,Penn团队早期的基因治疗工作使用了一种病毒载体,通过视网膜下注射将正常的RPGR拷贝特异性地传递给视杆细胞和视锥细胞。
在新发表的论文中,研究小组报告说,这种在狗5周大时进行的治疗成功地阻止了感光细胞的丧失,并使狗的视力保持了三年多的研究。
本研究还进一步进一步使用了相同的病毒载体和相同的方法,除了这次在两个稍后的时间点开始基因治疗干预:在12周龄,研究人员术语“中阶疾病”,约40%眼睛的光感受器细胞已经死亡,或者在26周龄,“晚期疾病”,当大约50%〜60%的杆和锥体丢失。
该团队对在这些后期治疗的担忧,视网膜可能在治疗沉积局注射后可能无法正确重新应变,并且可能存在毒性病毒载体由于感光细胞变性程度较大。在他们的随访中,他们没有发现任何一个问题的迹象。
Aguirre说:“我们花了很多时间来确保治疗基因在表达的时间和地点受到严格的控制。”“幸运的是,我们已经看到,这种疗法似乎在视网膜中有很好的耐受性。”
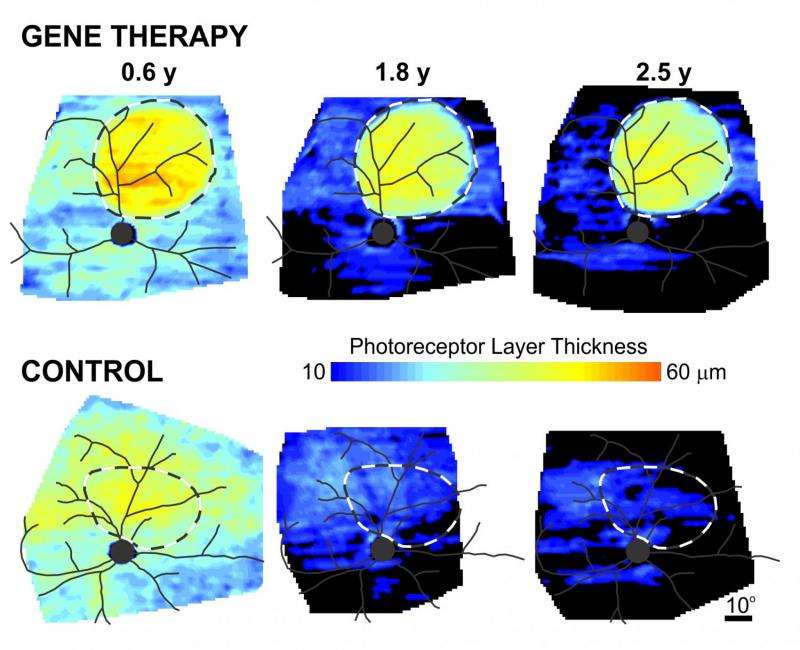
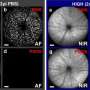
相反,他们所看到的是,在视网膜电成像和光学相干断层扫描成像等人类医学中使用的非侵入性测试中,视网膜治疗区域的光感受器细胞的退行性显著而持久的停止。在这些疾病晚期接受治疗的狗,甚至有一些杆状细胞和锥状细胞的结构异常逆转。这些发现转化为在视觉行为测试中的表现的提高,一个Y型迷宫测试狗是否能察觉昏暗的光线和一个障碍路线,以评估它们的视觉导航技能。在治疗晚期组,这些狗的表现至少持续了两年半,这是最新的时间点。
“对狗的研究表明,特别是那些在后期进行治疗的,你可以治疗一个相对较小的区域——视网膜表面的20%或更少,你已经有50%的感光细胞在治疗前死亡,但仍然看到不仅是电生理的改善和拯救,而且是视觉行为的实际拯救,”Beltran说。
“根据我的经验在佛罗里达大学的Hauswirth说:”基于我在动物模型中开发动物模型的基因疗法,“我认为这份报告描述了最强烈的案例,但最终在XLRP中的人类成功治疗。”
就像他们早期的工作一样,研究人员表明杆状细胞和锥状细胞的功能都得到了恢复,这些感光细胞与向大脑传递视觉信号的神经元正确连接。
Cideciyan说:“因为这是一种光感受器疾病,会影响视杆细胞和视锥细胞,也就是昼夜视觉细胞。能证明这两种细胞都获救了,真是太棒了。”
“我担心我的患者遗失了感光细胞并且可能在其视网膜中具有异常的连通性和结构,在疾病的后期阶段,基因治疗是否仍然适用于它们,“雅各布森说。”此处显示的是,治疗导致下游神经元是坚固和连接的,这是对最终的人类治疗非常重要。“
为了将这项工作带入人类治疗领域,研究人员正在对患者进行检查,以确定视网膜的哪个部位适合注射,以及哪些患者可能有资格进行最终的临床试验。他们也在研究在连接纤毛中与RPGR一起起作用的其他基因“伙伴”,看看是否有其他治疗目标。
进一步探索







用户评论