在牙釉质细胞形成过程中运输钙的细胞机制
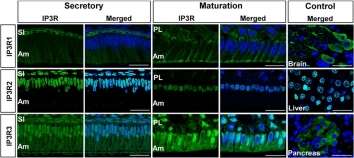
由Rodrigo Lacruz,MSC,博士学位领导的研究人员,博士学位,基础科学系基本科学和颅面生物学系助理教授发表了一篇论文科学报告(5:15803)标题为“牙釉质细胞表达功能SOCE渠道”,其报告了研究结果首次表现出牙釉质形成的钙转运机制。
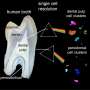
小组发现了主要的钙流入通道涉及矿化搪瓷[被称为CRAC (Ca2+释放激活Ca2+)通道——SOCE(商店经营的Ca2+进入)通道的主要类型——是控制钙摄取的关键,钙摄取对牙釉质的发展是必要的。尽管钙在牙釉质的发展中起着中心作用,但以前人们并不知道钙是如何从血液运输到牙釉质晶体生长的区域的。
由于控制这些通道的活性的基因中的突变,该发现对患有异常牙釉质的人具有重要意义。
拉克鲁兹博士说:“牙釉质的一个主要特征是它的持久性,这要归功于它所含的钙和其他矿物质的特别高的含量。”“但是钙必须到达晶体形成的区域。当形成CRAC通道核心的基因发生突变时,这种作用就会受到阻碍,牙釉质就会受到严重影响。”
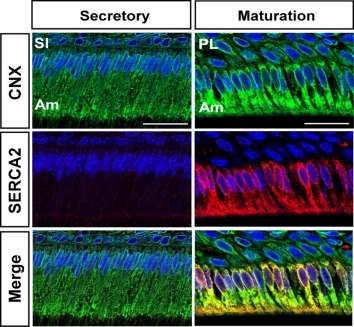
在这项研究中,包括Lacruz博士实验室的Meerim Nurbaeva博士和Miriam Eckstein博士在内的团队首次使用了啮齿类动物牙齿中新解剖的釉质细胞(成釉细胞)来调节生理过程,以了解CRAC通道在釉质钙信号传导中的作用。这项研究建立在之前的基因组研究的基础上,这些研究确定了参与牙釉质成熟阶段的基因,以及其他研究表明,基因ORAI1和STIM1 (CRAC通道的主要组成部分)的突变可以影响牙釉质发育。这项新的研究表明了钙内流在釉质细胞中的生理机制,并表明了它是如何被调节的。
Lacruz博士说:“通过关闭内质网中的钙泵,我们能够看到CRAC通道对钙吸收和信号传导的贡献,更具体地说,是它们如何调节釉质基因功能。”
首先在患有CRAC渠道的牙釉质矿化中参与牙釉质矿物质的基因突变在具有严重的综合免疫缺陷的人中,其中 - 其他症状牙釉质的疾病可能在出生后五或六年内脱落牙齿,以及牙本质变得暴露。这些严重遗传障碍的病例数量小于全球范围内,但根据突变发生的位置,个人可能会经历牙釉质伴有轻微或严重免疫缺陷的缺陷。此外,牙齿可能成为识别免疫系统缺陷的生物标志物。
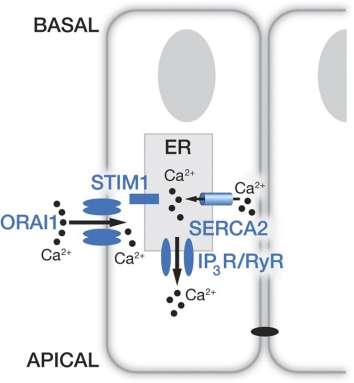
合著者之一,纽约大学医学院病理学系的Stefan Feske博士,在2006年发现了ORAI通道,它可以打开和关闭,让钙进入细胞。这一发现对于解决一个重要的谜团至关重要钙涌入在牙釉质矿化方面,Feske博士也发挥了重要作用。
钙储存在细胞的内质网(ER)中,直到它需要。在许多细胞中,蛋白质STIM1充当内质网的传感器,确保内质网内钙的平衡,并在钙水平低时发出警报。STIM1与细胞膜上的ORAI通道相互作用,允许钙从血液进入细胞恢复平衡。釉质缺损可由影响内质网或细胞膜上ORAI通道的STIM1钙传感器的基因突变引起。
根据Lacruz博士的说法,牙釉质生物学的这一新前沿使再生牙釉质的可能性更接近现实,从长远来看,这将有利于那些患有牙釉质形成障碍的人。“你需要知道所需的成分和钙运输的机制。这项研究很可能会对组织再生领域做出贡献。你必须知道组织是如何工作的,才能模拟其特性。”
进一步探索












用户评论