发现差异化的新途径,在一些癌症上脱落

在人类中,干细胞分化为数百种专业细胞类型至关重要。差异化驱动从受精卵到新生儿的发育,它是在成年人中每小时死亡的50亿细胞的连续替代。在下行,不同细胞类型的分化途径的突变可以是癌症的驱动因素。
信阳赵,博士及其同事李章,伯明翰大学李章,七位七位七位其他机构发现了一种新的差异机制,如巨大的统计,所以血细胞负责血小板生产。
这种机制可以提供新的研究和治疗方法,对血恶性肿瘤以及结肠和乳腺癌等实体肿瘤。由于途径-PRMT1和RBM15中的两种关键蛋白质在所有组织中表达,因此它们还可以调节其他组织中的分化,特别是那些RBM15已被证明对发育至关重要的分化,包括心脏,脾脏和胎盘。
控制祖细胞的决定的机制在通往小区专业化的道路上拍摄一个叉子或另一个叉子是理解分化的关键。由于PRMT1和RBM15在植物,两栖动物,鱼类,鸟类和哺乳动物中高度保守,新途径可能参与这些不同的生物。每个有机体都有很多专业化细胞类型,但所有专门的人细胞出现较少专业化祖细胞这可以分配成各种专用细胞。在人类中的一个例子是骨髓中的血液干细胞,可以专门化为十几种不同的血细胞红细胞、中性粒细胞或自然杀手细胞。每天都会产生数十亿的专门血细胞。
赵某和他的同事于在Elife印刷出版的工作,已经进行了四年。
该途径是复杂的,但其最终效果是信使RNA的替代剪接 - 特别是称为转录因子的主调节因子的信使RNA。这些因素控制了从DNA基因的遗传信息读取遗传信息,并充当所有生物体中的开关来控制基因表达。虽然神经细胞和肌肉细胞具有相同的基因组,但是,不同的基因表达给出了其截然不同的品质。
通路的细节
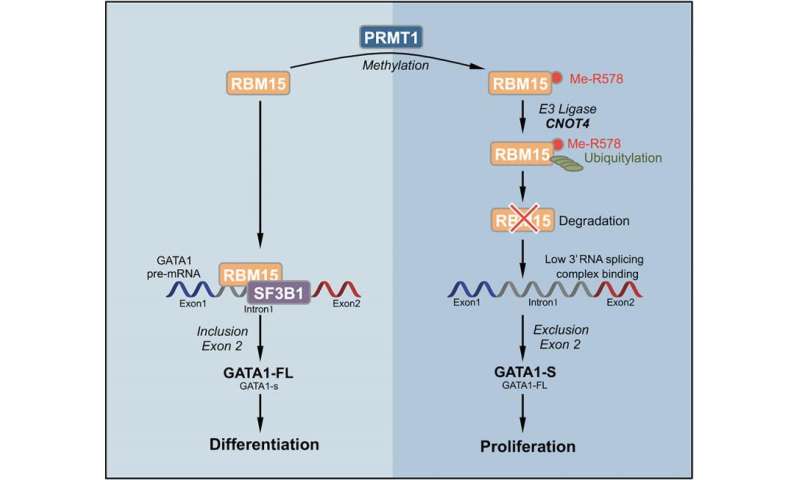
途径从甲基转移酶酶PRMT1开始。该酶将甲基附着在靶蛋白的特异性精氨酸氨基酸残基上。Zhao团队筛选蛋白质,通过PRMT1用甲基标记,并选择其中一种 - RNA结合蛋白RBM15-进一步研究。RBM15是兴趣的,因为RBM15和MKL1蛋白的突变融合与急性巨核细胞白血病有关。
在实验中,赵和同事发现,当细胞中prmt1水平高时,在某些精氨酸残基上用甲基标记更大比例的RBM15。该标记导致称为CNOT4的连接酶与另一个标签,泛素 - 标记RBM15,泛素 - 标记为蛋白质用于运输到细胞的垃圾去除机制的众所周知的信号,其中蛋白质降解和再循环。赵的团队发现,即使RBM15 mRNA的量没有变化,甲基标记的RBM15蛋白也迅速消失。因此,PRMT1的表达水平反常影响RBM15蛋白的量。虽然以前已知通过磷酸化和赖氨酸甲基化触发蛋白质泛醌,但是通过精氨酸甲基化的这种触发是未知的。
当RBM15蛋白的浓度低时,巨核细胞祖细胞不能向前移动以分化。当RBM15的浓度足够高时,祖细胞经历分化为成熟的巨核细胞,该专用血细胞在哺乳动物中产生血液凝血血小板。
要了解该开关功能,需要简要说明RNA拼接。在细胞核内,通过DNA序列编码基因。将该基因序列复制到RNA的一股RNA中,然后通过核糖体处理,以构建由DNA编码的蛋白质。核糖体的RNA碱基序列的读数告诉核糖体,氨基酸序列逐一的序列加入以构建蛋白质。但存在并发症:DNA基因序列,因此RNA副本也含有称为内含子的非读数插入物。在核糖体可以制备蛋白质之前,必须通过RNA剪接酶切出这些内含子。当它们移除内含子时,剪接酶加入读取序列的末端,称为外显子。这为核糖体产生了适当的信使RNA。
因此,一个带有三个外显子和两个内含子的基因类似于这句话:“The quick red xxxxxxxxxx fox jumps over yyyyyyyyyy The lazy brown dog.”(快速的红色xxxxxxxxxx狐狸跳过了懒棕色狗)。剪接完后,留言就会这样写:“敏捷的红色狐狸跳过了懒惰的棕色狗。”当内含子被移除时,这些外显子需要被拼接在一起。
Zhao和同事发现,RBM15 RNA结合蛋白结合到在巨核细胞分化中重要的基因的前信使RNA的内含子区域,包括三个转录因子,如RUNX1, GATA1和TAL1,在正常和异常的造血过程中是重要的。RBM15似乎招募了剪接因子SF3B1来正确剪接外显子。当RBM15低时,一个或多个外显子没有正确剪接。因此,这是一种新的细胞分化机制,由rna结合蛋白的甲基化启动。
“RBM15通过SF3B1的替代剪接的调节是一种令人兴奋的和新的途径,清楚地参与巨大细胞的决定来生长或区分,”血液学/肿瘤学教授,生物化学和生物化学和分子遗传学,在西北大学Feinberg医学院。“这些发现表明,通过抑制PRMT1活性调节RBM15活性可以改变巨核细胞肿瘤细胞的拼接模式,并促进其分化。”
更广泛的作用?
RBM15可能在细胞中具有更广泛的功能,说赵和同事。他们发现RBM15直接与1,257个基因的前信使RNA结合。其中是参与代谢调节的基因。同意这种发现,赵和同事发现,PRMT1的过度表达或RBM15的表达减少增强了更多线粒体的产生,细胞的动力静脉。与Minkui Luo,Ph.D的纪念斯隆静脉癌中心实验室合作,Zhao的组进一步确定了白血病细胞中PRMT1调节的代谢途径。在制备的稿件中,这些数据将进一步将肿瘤内酯联系起来给代谢途径。
替代RNA剪接在癌症研究中引起了关注。70%以上的骨髓增生异常综合征患者和20%的慢性淋巴细胞白血病患者中存在剪接因子SF3B1突变,突变的SF3B1也出现在其他类型的血液系统恶性肿瘤中。了解PRMT1- rbm15轴可以为sf3b1突变的血液恶性肿瘤提供新的线索,并可能导致靶向PRMT1作为骨髓增生异常综合征的一种新的治疗方法。在与乔治亚大学的Y. George Zheng博士的长期合作中,Zhao的团队一直在测试PRMT1抑制剂。















用户评论