研究确定了司机,潜在的目标积极小儿白血病亚型
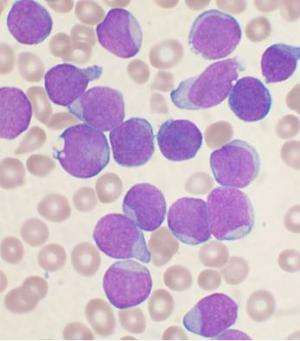
科罗拉多大学癌症中心的一项研究计划于2月18日,2016年在线发表在《华尔街日报》细胞的报道模型早期t细胞前体急性淋巴细胞白血病(ETP-ALL),发现失活基因EZH2的司机和减少潜在疾病的治疗目标。
“大约15%的急性淋巴细胞白血病来自儿童t细胞前体。我们知道,所有患者需要更多的治疗的前期,我们必须打击的难度。当这种形式的疾病复发,或不响应建立治疗,很难治疗。ETP-ALL亚型t经常出现的行为在这个问题的方式,”托拜厄斯。内夫说,医学博士,研究员铜癌症中心,在科罗拉多州儿童医院儿科肿瘤学家。
在《华尔街日报》2012年的一篇论文自然,描述大规模测序研究儿科ETP-ALL,显示一个复杂的混合基因改变的两个主要结果:ETP-ALL显示频繁突变分子调节生长和存活的信号,和超过40%的ETP-ALLs灭活基因EZH2的改变。EZH2损失函数可以依次灭活所谓Polycomb压制复杂2 (PRC2)。
然而,如何Polycomb压制复杂2损失函数突变有助于白血病增长2012自然研究的还不清楚。当前的研究从科罗拉多大学癌症中心现在揭示了这个问题。
ETP-ALL以前已知干细胞的基因表达。内夫,连同co-first艾蒂安Danis作者,博士,助理研究员在儿科铜医学院和他的同事,现在表明,从干细胞分化成更专门的血液细胞部分取决于EZH2 / PRC2,直接连接PRC2失去干ob体育开户网址细胞的功能基因表达谱。
“干细胞的基因表达谱如何有助于ETP-ALL侵略性的急性白血病是未知的,但是我们知道,这些干细胞样细胞与不良预后相关急性白血病”,内夫说。
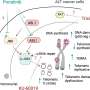
EZH2失活的另一个后果是增加了生长和存活信号。在健康组织,白介素6细胞生长的信号,例如损伤后组织修复的目的。在ETP-ALL,白介素6细胞变得特别敏感,使这些细胞增长远远超出健康同行。当前的研究支持Ezh2酶热刺的概念,损失增长通过增加细胞受体的表达白介素6。
“我们有两个主要功能的疾病——干细胞样细胞,增加——现在我们显示一个演员参与,即EZH2 / PRC2”内夫说。
事实上,基因EZH2和酶解机制EZH2编码将会超出ETP-ALL。酶是早期的球员在一个复杂的细胞网络通信,还参与其他一些影响儿童和成人疾病,包括神经纤维瘤,少年myelomonocytic白血病和骨髓增生异常综合征。
内夫表明考虑Ezh2作为一个演员在许多条件说明了现代科学范式转换的方式评估疾病,从模型的病理学家定义疾病的形态外观模型的疾病是由其基因签名。疾病在显微镜下这段看起来不同,但这项工作表明他们可能由于基因密切相关。
“除了我们特定的发现在这种疾病,我们兴奋现在有一个模型,允许我们探索的后果Ezh2失活可能丰富我们的理解许多其他条件相似的基因改变,”内夫说。
集团计划使用新开发的老鼠模型来测试疗法对抗的结果Ezh2失活。具体地说,本文表明,现有的药物ruxolitinib插手信号链中的重要一环,可能由Ezh2失活。用这个链接(即JAK-STAT信号)由ruxolitinib沉默,白血病细胞的小鼠模型显示增长延迟。
“Ruxolitinib本身不太可能治疗该疾病,但这个模型将帮助我们测试可能的药物组合,最终可能ETP-ALL患者受益,”内夫说。
在未来的研究中,该组织计划使用先进的遗传和化学筛选功能在科罗拉多大学的系统测试与灭活Ezh2许多药物对细胞的活动。