干细胞基因治疗可能是治疗杜氏肌萎缩症的关键
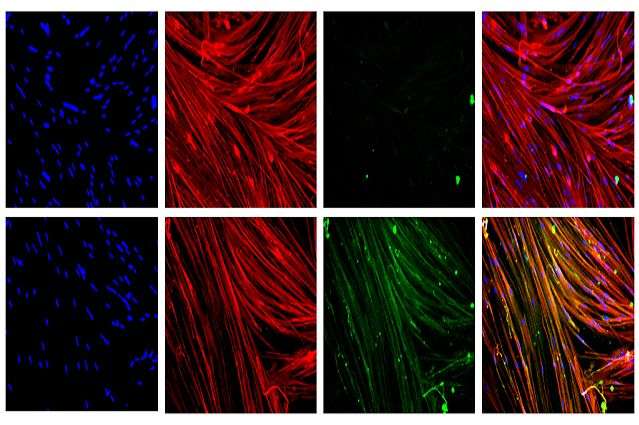
加州大学洛杉矶分校Eli和Edythe Broad再生医学和干细胞研究中心以及杜氏肌营养不良中心的科学家们开发了一种新方法,最终可以用于治疗杜氏肌营养不良。干细胞基因疗法可能适用于60%的杜氏症患者。在美国,大约每5000名男孩中就有1人患有杜氏症,这是最常见的致命儿童期遗传疾病。
该方法使用一种名为CRISPR/Cas9的技术来纠正导致该疾病的基因突变。该研究由共同高级作者阿普丽尔·派尔、梅丽莎·斯宾塞和第一作者考特尼·杨领导,发表在该期刊上细胞干细胞。
研究人员设计了这种方法,以便将来在临床中使用。
加州大学洛杉矶分校大卫·格芬医学院的神经学教授斯宾塞说:“这种方法要在人体上进行测试可能还要10年。”加州大学洛杉矶分校杜氏肌萎缩症中心的联合主任和布罗德干细胞研究中心的成员“重要的是,我们采取所有必要的步骤来最大限度地提高安全性,同时迅速将治疗方法带到临床试验中。”
杜氏症通常是通过一种叫做抗肌萎缩蛋白的基因的突变发生的,这种基因会产生一种同名的蛋白质。在没有这种疾病的人身上肌营养不良蛋白的蛋白质帮助加强和连接肌肉纤维细胞。抗肌萎缩蛋白基因中有数百种突变会导致这种疾病,但在60%的杜兴氏症患者中,他们的突变会发生在基因的特定热点内。
杜氏突变会导致肌营养不良蛋白的产生异常低,进而导致肌肉退化并逐渐变弱。症状通常开始于儿童早期;患者逐渐失去活动能力,通常在20岁左右死于心脏或呼吸衰竭。目前的一些药物可以治疗这种疾病的症状,但没有一种药物可以阻止疾病的发展或显著提高患者的生活质量,目前也没有办法逆转或治愈这种疾病。
聚焦热点
加州大学洛杉矶分校的研究人员开发的平台专注于抗肌萎缩蛋白基因的热点。
为了测试这个平台,他们从杜氏肌萎缩症中心(Center for Duchenne Muscular dystrophphy)同意的患者那里获得了皮肤细胞,这些患者都有肌萎缩蛋白基因热点内的突变。研究人员对这些细胞进行了重新编程,使其产生诱导多能干细胞在布罗德干细胞研究中心的一个符合fda规定的设施;该设施的使用是临床前研究向人体临床试验过渡过程中的重要一步。诱导多能干细胞,或称iPS细胞,有能力成为任何类型的人体细胞,同时还能保持其来源人的遗传密码。
接下来,科学家们利用他们开发的使用CRISPR/Cas9技术的基因编辑平台去除iPS细胞中的杜兴突变。(CRISPR的意思是“定期聚集的间隔短回文重复”。)该平台瞄准并去除营养不良基因热点的特定区域,该基因含有60%的杜兴突变,恢复缺失的蛋白质。
CRISPR/Cas9是细菌用来对抗病毒的一种自然反应。2012年,科学家们发现他们可以利用这一过程来切割特定的人类DNA序列。CRISPR/Cas9系统的一部分就像一个导航系统,可以通过编程找出遗传密码的特定部分,比如一个突变。该系统的第二部分可以从遗传密码中去除突变,在某些情况下可以用正常的遗传序列来替换突变。
加州大学洛杉矶分校的研究人员一旦培育出不受杜兴突变影响的诱导多能性细胞,他们就将诱导多能性细胞分化成心肌和骨骼肌细胞,然后移植骨骼肌细胞植入抗肌萎缩蛋白基因发生突变的老鼠体内。
他们发现移植的肌肉细胞成功地产生了人体抗肌萎缩蛋白。
这是使用CRISPR/Cas9观察到的dystrophin基因中最大的缺失,该研究也是首次创造出可以直接恢复受Duchenne影响的功能性肌肉组织的修正的人类iPS细胞。(此前,科学家们曾使用CRISPR/Cas9修复影响少数杜氏症患者的突变,以及不一定与临床相关的细胞类型。)
“这项工作证明了使用单基因编辑平台的可行性,再加上干细胞为60%的杜兴患者纠正基因突变和恢复抗肌萎缩蛋白的生产,”微生物学、免疫学和分子遗传学副教授、布罗德干细胞研究中心成员派尔说。
个人联系
杨是加州大学洛杉矶分校的博士前研究员,也是加州大学洛杉矶分校一个名为“杜兴布鲁恩联盟”的学生组织的主席。她对杜兴研究特别有热情,因为她有一个表亲患有这种疾病。
“我已经知道我对科学感兴趣,所以在我表弟被诊断出患有杜兴病后,我决定把我的事业奉献给寻找杜兴病的治疗方法,”扬说。“知道我正在做一些事情来帮助所有想要追杀我表弟的男孩,这让一切都变得更有意义。”我觉得自己在做出贡献,我很兴奋,因为杜兴的研究领域正在朝着真正积极的方向发展。”
杜氏营养不良症肌肉萎缩症是30种肌肉萎缩症中最常见和最严重的一种。
加州大学洛杉矶分校的研究人员计划开发测试杜兴特异性CRISPR/Cas9平台的策略,以治疗动物疾病,作为完善可用于人类的方法的下一步。
加州大学洛杉矶分校的科学家们为杜兴开发的CRISPR/Cas9平台目前还没有上线临床试验而且还没有被FDA批准用于人体。
进一步探索













用户评论