当线粒体在线粒体中的钙使用者心脏功能障碍时,压力推动细胞死亡
发病性的线粒体 - 细胞的发电厂 - 是由中风,心脏病发作和神经变性疾病引起的损害,但如何阻止这些反应器熔化,破坏细胞和组织甚至很少。线粒体还占用钙,调节能源生产。现在,在线自然通讯美国托马斯·杰斐逊大学(Thomas Jefferson University)的研究人员发表了一份重要的研究报告,揭示了线粒体是如何自然保护自己,避免摄入过多钙的,因为过量钙会导致细胞死亡。
Their findings offer a novel avenue for creating drugs designed to stop mitochondria from demolishing cells during a time of stress, such as from a heart attack, says one of the study's senior authors, Professor György Hajnóczky, M.D., Ph.D., director of the MitoCare Center at Thomas Jefferson University.
“线粒体失败导致心脏病和大脑中看到的大部分伤害在攻击和中风中,并抑制了短暂的过载钙我们在这些事件中看到的,可以大大减少长期损坏,“他说。”这可能成为一种新颖而令人兴奋的待遇战略。“
研究人员表示,最终可以开发线粒体治疗以帮助治疗神经变性疾病,其特征是具有功能失调的能量生产。
线粒体研究最近经历了一次复兴,导致2014年杰斐逊大学(Jefferson University)的线粒体护理中心(MitoCare Center)成立。线粒体不仅为维持生命的细胞机制提供大量能量,而且研究人员发现,它们还有助于细胞理解环境信号,这些信号可以改变细胞的行为。他们还意识到,线粒体功能障碍可能是细胞死亡的信号,这是一系列疾病的基础。
在这项研究中,以博士为首的四个研究小组。György Csordás, György Hajnóczky, Jan Hoek和Erin L. Seifert,都来自mitcare中心,他们用细胞和动物研究来研究弯曲的细胞内和外钙的流动发电厂。
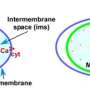
几年前,Hajnóczky博士和他的团队揭示了Micu1(线粒体钙吸收1)的功能。他们发现该蛋白质控制允许钙进入线粒体的通道(MCU,线粒体钙钙钙)。MICU1充当门守防止连续摄入,但允许钙信号增加能源生产。
目前研究项目的目标是了解MICU1的生理和病理作用。找出线粒体时会发生什么钙吸收由于MICU1没有得到适当的调节,研究人员开发了MICU1缺失的第一个动物模型。他们发现没有MICU1的小鼠在子宫内发育正常,但出生后不久就死亡了。“这些幼犬无法应对从宫内生活到宫外生活的压力,”Hajnóczky医生说。
然后,它们开发了仅在肝脏中仅移除Micu1的成年小鼠,该器官可以在损坏时通常再生。在这些小鼠中发现的研究人员发现肝脏的基本功能很好,但是当肝脏暴露于应激时(一部分被手术被移除),肝脏不能再试,因为它通常是因为过多的钙流入细胞线粒体,触发组织死亡。“当强调时,没有Micu1钙守门人,肝细胞死亡,”Hajnóczky博士说。
“心脏、大脑和肝脏都非常依赖能量,如果线粒体功能失调,它们很快就会陷入麻烦,”他说。“例如,心脏病发作时心脏细胞突然缺氧,中风时脑细胞突然缺氧,也代表线粒体受到压力。”由于随之而来的能量不足,钙在细胞中积累,线粒体被钙淹没。如果线粒体不能控制这些钙,它们就会分解导致细胞去死。
“也有迹象表明线粒体钙失调在各种神经退行性疾病,包括阿尔茨海默病,亨廷顿的疾病和娄盖克氏症的疾病,“Hajnóczky博士补充道。”这些疾病并不一定在线粒体中开始,但它们引起的损害在这些细胞器中被扩增。“
“抑制线粒体钙的摄取作为短期治疗可以为急性心脏和脑攻击提供真正的承诺。在复杂和慢性神经变性中仍然是不可预测的,无论对钙吸收的简单抑制都是有效的。相反,相当强化复杂的守门社以及钙信号Micu1的功能可能是明智的,“他说。
该团队已经开始筛选潜在的制剂,同时继续梳理MICU1生物学的生物学根源。
进一步探索






用户评论