科学家发现了个性化、功能性胰岛素生成细胞的“秘方”
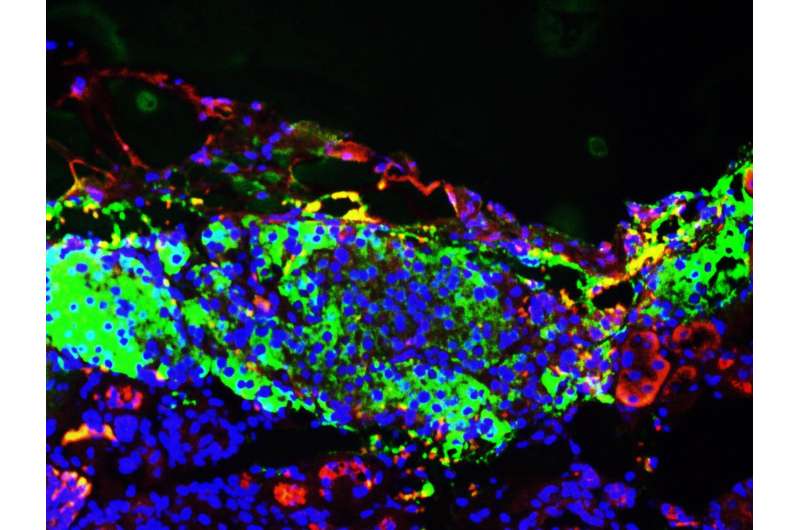
索尔克的科学家们已经解决了为糖尿病患者创造替代细胞的长期难题。研究小组发现了一个隐藏的能量开关,当它被翻转时,就会增强胰腺细胞对葡萄糖的反应,这是之前研究没有发现的一步。其结果是产生了数亿个实验室生产的人类β细胞,能够缓解小鼠的糖尿病。
十多年来,世界各地的科学家都在努力取代失败胰腺细胞与儿童免疫破坏有关(1型糖尿病)或成人肥胖相关糖尿病(2型糖尿病)。尽管在培养皿中培养的细胞能够产生胰岛素,但它们对葡萄糖反应迟缓或根本无法做出反应。
索尔克基因表达实验室的高级合著者和主任罗纳德·埃文斯说:“我们发现了产生强健和功能正常的人类β细胞所需的缺失的能量开关,有可能将这一发现转化为人类糖尿病的可行治疗方法。”那部新著作发表于细胞代谢2016年4月12日。
索尔克技术从诱导开始多能细胞iPSC是一种干细胞技术,病人的组织(如皮肤)被重新编程成其他类型的细胞,如胰腺。这一步产生前细胞,它产生胰岛素,但还没有功能。虽然有几个研究小组达到了这个节点,但通往功能细胞的道路并不清楚。

“胰腺β细胞必须能够做两件事才能有效地工作:对葡萄糖做出反应和产生胰岛素,”埃文斯说,他也是霍华德休斯医学研究所的研究员和分子与发育生物学的March of Dimes主席。“没有人能弄清楚如何制作胰腺细胞到目前为止,人类患者可以做到这两点。”
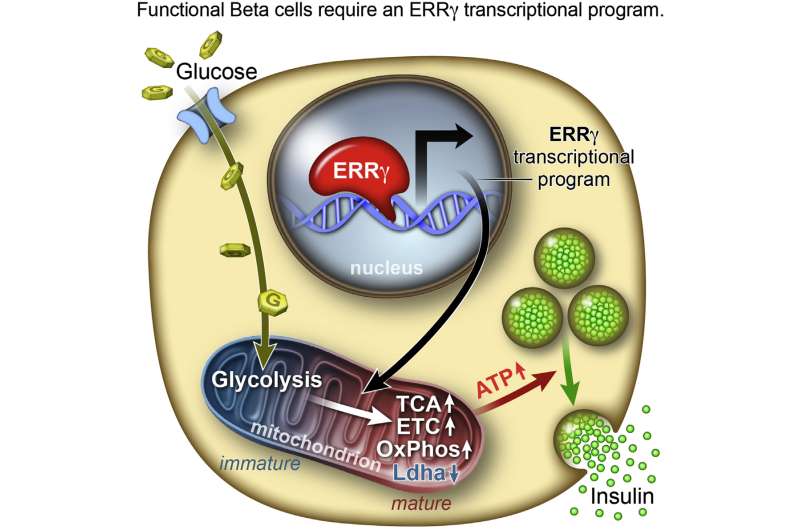
索尔克团队仔细研究了β细胞的基本生物学,并发现了几个被称为转录因子的分子开关,它们被关闭,但可能控制着向完全功能状态的转变。索尔克研究小组发现,这个“秘密武器”是埃文斯实验室多年来一直在研究的一个特殊开关,它在细胞信号传递中所起的作用。这种蛋白质开关被称为r -gamma,对于唤醒沉默的β样细胞至关重要,这些细胞现在可以对葡萄糖做出反应并相应地释放胰岛素。
“这一进步将导致比目前可用的治疗方法更好地控制胰岛素反应,”联合资深作者、索尔克高级科学家迈克尔·唐斯说。“以前对β细胞的成熟过程一无所知。我们偷看了那个黑匣子,现在我们知道发生了什么。”他补充说,该团队的技术是一种简单、快速和廉价的方法,可以在与患者基因匹配的培养皿中制造可移植的人类胰腺β细胞。
“当我们在培养皿中向糖尿病前期β细胞中添加r - γ时,我们成功地创造了一个葡萄糖反应的β样细胞,”论文第一作者、索尔克研究助理Eiji Yoshihara说。“当我们从动物体内去除r - γ时,葡萄糖反应就被消除了,这证明了该因子是β细胞成熟的主要调节因子。”
但是这些β细胞能成功治疗糖尿病吗?索尔克的研究人员发现,确实,当它们成熟时β细胞将其移植到1型糖尿病小鼠体内,该手术迅速挽救了它们的糖尿病。埃文斯说:“希望这能反映出临床中会发生的情况——在有人被诊断患有糖尿病后,他们可能会得到这种治疗。”“这很令人兴奋,因为它表明培养皿中的细胞已经准备好了。”
研究人员希望在未来几年内进行人体试验。
更多信息:细胞代谢, Yoshihara等人:“ERRγ是治疗功能葡萄糖反应β细胞代谢成熟所必需的。”dx.doi.org/10.1016/j.cmet.2016.03.005