癌细胞相互协调形成流动的群集
据莱斯大学的科学家称,癌细胞之间的双向交流似乎是它们通过转移而变得活跃、聚集和扩散的关键。
莱斯大学理论生物物理中心的成员开发了一种模型,描述癌细胞如何扭曲复杂的信号和反馈回路系统,使之对自己有利。这些信号帮助细胞从原发肿瘤中分离出来,形成群集,导致通常致命的转移性疾病。
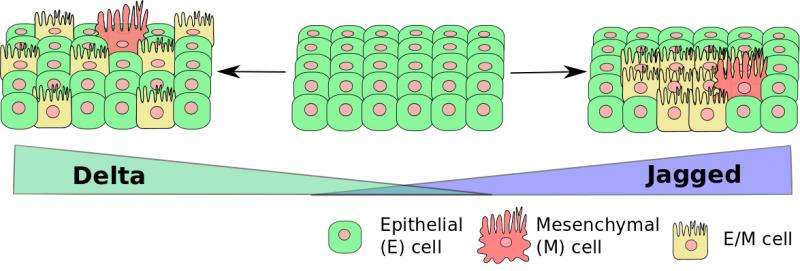
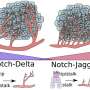
莱斯大学团队2015年报告这一notch信号途径,涉及蛋白质被称为“缺口”,“锯齿”和“三角洲”可以被劫持癌细胞.在正常手术中,该机制对胚胎发育和伤口愈合至关重要,通常在delta时激活配位体一个细胞的notch受体与另一个细胞的notch受体相互作用。他们的新论文发表在英国皇家学会杂志上接口提出了癌症细胞使用这些蛋白质,特别是锯齿状蛋白质,不仅可以建立双向信号,将它们转变为混合上皮细胞间充质细胞也可以形成移动的集群。
赖斯大学理论生物物理学家赫伯特·莱文说:“总的来说,我们的兴趣一直在于细胞在离开原发肿瘤时所做的决定。”“上皮细胞原发肿瘤均为异常。尽管如此,他们看起来像正常细胞即使它们长在了不该长的地方。但只有当细胞离开并在身体的其他地方开始新的生长时,癌症才会变得真正致命。”
因为notch信号这样一个常见的功能,研究人员怀疑它可以被重新利用流氓细胞.“在过去的几年里,我们一直认为细胞会主动决定细胞命运,变得有活力并离开肿瘤。这篇论文阐述了细胞之间协调决策的程度,”他说。
Levine、莱斯大学的同事José Onuchic和前莱斯大学研究员Marcelo Boareto领导的这项研究为癌症研究人员在寻找破坏转移过程的方法时提供了一个新的考虑目标。
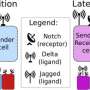
Notch信号在一个细胞中开始触发邻近细胞的转变,例如,允许干细胞重新配置它的一个邻居以实现特定的功能。“你有作为发送者的细胞和作为接收者的细胞,”Onuchic说。“通过这样做,它们可以进行微分.他们可以让自己的伴侣与自己不同。”
但在癌症中,细胞可以同时充当接收者和发送者,特别是当它们将初级配体改变为锯齿状时。“事实证明,锯齿状增长是确凿的证据,”他说。他说,锯齿状蛋白质的数量增加不仅有助于创造这些活动的杂交细胞,还有助于杂交细胞交换信息,以确保所有能够聚集成一个群体的细胞。
“生物学家通常不会考虑配体之间的差异,”Boareto说。“但两者有很大的不同。这篇论文的主要信息很简单:Notch-delta信号导致孤立的细胞经历损伤epithelial-mesenchymal过渡(EMT)转变为活动个体,锯齿状缺口导致细胞群经历EMT转变为活动集群。”
研究人员怀疑这种转变不是随机的。莱文说:“现在我们知道它们不仅仅是对环境的反应。”“它们通常是由于细胞之间的交流和集体决策。”为了验证这些想法,他说,德克萨斯大学MD安德森癌症中心的合著者Sendurai Mani将在未来几年内使用癌症组织样本来量化锯齿状蛋白和其他相关蛋白的存在。
奥努奇克说,这并不奇怪细胞使用缺口路径,也可能使用其他路径。“癌症从来没有在生物学上创造出一个全新的机制,”他说。“它利用现有机制来满足其需求。了解这一过程可以为预防转移提供新的线索。”
即使这一发现不能立即应用于治疗,它也可以通过量化notch蛋白、锯齿蛋白和delta蛋白的表达来帮助诊断肿瘤的严重程度。“这给了我们一些衡量的东西,以更准确地预测癌症的危险程度原发肿瘤是,”莱文说。
进一步探索









用户评论