2型糖尿病药物试验不必要地将女性排除在外
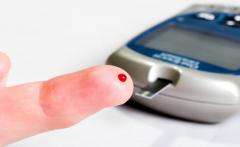
虽然孕妇、哺乳期妇女或可能怀孕的妇女通常被排除在2型糖尿病药物的临床试验之外,但这种排除往往不是基于胎儿损害的风险,据宾夕法尼亚州立大学医学院的研究人员称,这可能是导致临床试验中女性比例不足以及对药物对意外怀孕女性的影响不完全了解的原因。
以前的研究表明,在临床试验中女性的代表性不足。限制注册的限制孕妇和有生育潜力的妇女至少对这种差距负有部分责任,尽管国家卫生研究所1993年的一项规定指出,有生育潜力的妇女不应经常被排除在国家卫生研究所资助的临床研究之外。虽然有几项研究关注了基于现有怀孕情况的临床试验登记限制,但很少有研究关注可能怀孕的女性所面临的障碍。
为了调查登记限制,研究人员研究了在育龄妇女中非常普遍的2型糖尿病。
宾夕法尼亚州立大学医学院(Penn State College of Medicine)大三学生阿兰娜·l·费兰(Alannah L. Phelan)与妇产科和公共健康科学教授理查德·s·莱格罗(Richard S. Legro)合作,分析了在宾州大学注册的近700项2型糖尿病药物试验的数据ClinicalTrials.gov。这些研究可以追溯到1995年,至少包括一些18到40岁的女性参与者。费兰和勒格罗发现,59%的研究包含了至少一项与女性生育相关的排除标准。
“我们发现育龄妇女参与临床试验存在广泛的限制,”费兰说。
该标准通常排除正在怀孕或哺乳的妇女。
然而,超过50项研究排除了所有有生育潜力的女性。
研究人员报告说,特别严格的标准,如排除计划捐献卵子的妇女、要求两种避孕措施和在试验结束后要求避孕措施,并不少见,而29种试验需要多次怀孕测试才能继续参与试验。
研究人员随后试图了解排除有生育潜力的女性的标准是否与药物风险相称。
直到2015年,美国食品和药物管理局(Food and Drug Administration,简称fda)使用“A、B、C、D、X”类别系统对药物导致出生缺陷的风险进行分级,从最低风险的A类到最高风险的X类。
包括妊娠禁忌的X类药物在内的试验在目前的研究中是最受限制的。然而,排除标准并没有随着药物风险的增加而逐步增加,Legro说。研究人员发现,B类药物的试验比C类药物的试验更有可能排除正在怀孕或需要避孕的妇女,C类药物可能具有更大的胎儿风险。
费兰说:“这与药物风险和试验限制没有任何密切的联系。”
由研究者发起的试验——通常是在学术健康中心——倾向于更严格的限制,需要更多的避孕措施的使用,并且比药物公司的研究排除更多的女性。
研究人员推测,对责任的担忧导致了与实际风险不成比例的限制。研究人员在发表在该杂志上的论文中写道,尽管责任是一个合理的担忧,但它并不能取代临床研究中的公平和获取原则糖尿病护理。
以前的研究表明,如果给予机会并提供适当的信息,许多孕妇会选择参加临床试验出于个人和利他的原因。
莱格罗说:“对妇女参与临床药物试验仍然存在广泛的限制,而且往往没有正当理由。”“这些试验的结果可能不适用于更大范围的人群。多达一半的怀孕是计划外的,我们不知道这些药物会有什么影响女性如果她们在怀孕期间怀孕或者怀孕。”
进一步探索










用户评论